题目内容
3.将一小段镁带投入盛有稀盐酸的试管中,发生剧烈反应.一段时间后,用手触摸试管外壁感觉烫手.这个实验事实说明该反应( )| A. | 为放热反应 | |
| B. | 为吸热反应 | |
| C. | 反应过程中热能转化为化学能 | |
| D. | 反应物的总能量低于生成物的总能量 |
分析 用手触摸试管外壁感觉烫手,说明温度高于常温,为放热反应,结合反应物、生成物能量的关系解答该题.
解答 解:一段时间后,用手触摸试管外壁感觉烫手,说明反应为放热反应,则反应物的总能量高于生成物的总能量,将化学能转化为热能,
故选A.
点评 本题考查化学反应与能量,为高频考点,侧重于学生的分析能力和基本概念的理解和运用的考查,注意相关概念的理解学习,难度不大.

练习册系列答案
相关题目
11.下列各组有机物只用一种试剂无法鉴别的是( )
| A. | 乙醇、苯、四氯化碳 | B. | 苯、甲苯、环己烷 | ||
| C. | 苯、苯酚、己烯 | D. | 苯、乙醛、乙酸 |
18.以下说法中,不违背科学规律的是( )
①改变核外电子数可使原子与离子相互转化
②改变核内中子数可使不同的同位素相互转化
③改变核内质子数可使不同的元素相互转化,属于化学变化
④改变离子的电荷数可使一种元素的阳离子转化为另一种元素的阴离子.
①改变核外电子数可使原子与离子相互转化
②改变核内中子数可使不同的同位素相互转化
③改变核内质子数可使不同的元素相互转化,属于化学变化
④改变离子的电荷数可使一种元素的阳离子转化为另一种元素的阴离子.
| A. | ①② | B. | ②③ | C. | ③④ | D. | ①③ |
15.X、Y、Z、M、R、Q是短周期主族元素,部分信息如下表所示:
(1)R在自然界中有质量数为35和37的两种核素,它们之间的关系是互为同位素;R在元素周期表中的位置是第三周期ⅦA族.
(2)Z的单质与水反应的化学方程式是2Na+2H2O═2NaOH+H2↑.
(3)Y与R相比,非金属性较强的是Cl(填元素符号),下列事实能证明这一结论的是bc.(填字母序号)
a.常温下Y的单质呈固态,R的单质呈气态 b.稳定性XR>YX4 c.Y与R形成的化合物中Y呈正价.
| X | Y | Z | M | R | Q | |
| 原子半径/nm | 0.154 | 0.074 | 0.099 | 0.143 | ||
| 主要化合价 | -4,+4 | -2 | -1,+7 | +3 | ||
| 其他 | 阳离子核 外无电子 | 无机非金属材料的主角 | 焰色反应呈黄色 |
(2)Z的单质与水反应的化学方程式是2Na+2H2O═2NaOH+H2↑.
(3)Y与R相比,非金属性较强的是Cl(填元素符号),下列事实能证明这一结论的是bc.(填字母序号)
a.常温下Y的单质呈固态,R的单质呈气态 b.稳定性XR>YX4 c.Y与R形成的化合物中Y呈正价.
12.在一定体积的18mol•L-1的浓硫酸中加入过量的铜片,加热使之反应,被还原的硫酸为0.9mol.则浓硫酸的体积为( )
| A. | 等于50 mL | B. | 大于50 mL | C. | 等于100 mL | D. | 大于100 mL |
13.下列化学用语中,正确的是( )
| A. | 用电子式表示溴化氢的形成过程为: | |
| B. | 海水中Br-的电子式为: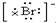 | |
| C. | 海水中通入氯气时发生反应的离子方程式为:2NaBr+Cl2=Br2+2NaCl | |
| D. | 氯离子的结构示意图为: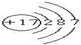 |

 有止血作用,特别对内脏的止血效果较好.
有止血作用,特别对内脏的止血效果较好. .
. .
.