题目内容
A、B、C、D、E是核电荷数依次增大的5种短周期主族元素;原子半径按D、E、B、C、A顺序依次减小,B和E是同主族元素。(1)下列推断正确的是_____________。
a.A、B、E不可能在同一主族
b.A、B、C可能在同一周期
c.C的最高价氧化物的水化物可能显碱性
d.C和D的单质可能生成离子化合物
(2)若A与D同主族,B是形成化合物种类最多的元素,C原子的最外层电子数比A与B的最外层电子总数还多1。则A与C元素按原子个数比2∶1形成的化合物F的电子式为_____________,C与D形成的原子个数比为1∶1的化合物与F反应的化学方程式_____________,由A、B、C、D四元素形成的无机化合物水溶液呈___________性(填“酸”或“碱”),离子反应方程式为_____________________________________________________。
(1)ad
(2)![]()
2Na2O2+2H2O=4NaOH+O2↑ 碱 ![]() +H2O
+H2O![]() H2CO3+OH—
H2CO3+OH—
解析:(1)(a)推断,若A、B、E位于同一主族,则它们只能位于第ⅠA族,A为H,B为Li,E为Na,核电荷数介于B、E之间的C、D位于第二周期,此时C、D原子半径比位于第三周期的E(Na)半径小,与题给条件不符,故A、B、E不可能位于同一主族,a推断正确。(b)推断,核电荷数依次增大的A、B、C若位于同一周期,则它们必从左到右依次排列,原子半径A>B>C,与题给条件不符,b推断错误。(c)推断,核电荷数比E少而原子半径比E大的D只能与E位于同一周期且在E的左边,核电荷数比B大而原子半径比B小的C只能与B位于同一周期且在B的右边,B、E同主族,三者位置关系可表示为:
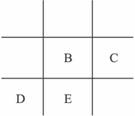
显然C不可能位于ⅠA或ⅡA,则C的最高价氧化物的水化物不可能显碱性,c推断错误。(d)推断,若D为Na,C为O,两者形成的Na2O为离子化合物,推断正确。(2)形成化合物种类最多的元素B是碳元素,核电荷数比B(碳)少且原子半径也比B(碳)小的A只能位于B(碳)的上一周期,则A为氢元素。与A(H)位于同一主族的D为Na,最外层电子数比A(H)与B(碳)最外电子总数还多1的C为氧元素。A与C按原子个数比为2∶1形成的化合物F为H2O,C与D按原子个数比1∶1形成的化合物为Na2O2;由A、B、C、D形成的化合物为NaHCO3。

 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案| A、简单离子的半径:C>D>E>B | B、工业上常用电解法制得C和D的单质 | C、稳定性:A2B>A2E | D、单质D可用于冶炼某些难熔金属 |

 2DB3,若3.2gDB2完全转化为DB3气体时放热akJ;1mol DB3气体完全转化为其水化物放热bkJ,则标况下33.6L DB2完全完成上述两步反应放热
2DB3,若3.2gDB2完全转化为DB3气体时放热akJ;1mol DB3气体完全转化为其水化物放热bkJ,则标况下33.6L DB2完全完成上述两步反应放热
