题目内容
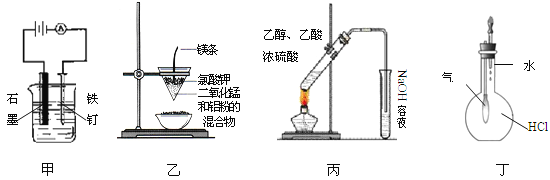
【题目】实验室制备硝基苯的实验装置如图所示(夹持装置已略去)。下列说法不正确的是( )

A.水浴加热的优点为使反应物受热均匀、容易控制温度
B.浓硫酸、浓硝酸和苯混合时,应向浓硝酸中加入浓硫酸,待冷却至室温后,再将所得混合物加入苯中
C.仪器a的作用是冷凝回流,提高原料的利用率
D.反应完全后,可用仪器a、b蒸馏得到产品
【答案】D
【解析】
A.水浴加热可保持温度恒定;
B.混合时先加浓硝酸,后加浓硫酸,最后加苯;
C.冷凝管可冷凝回流反应物;
D.反应完全后,硝基苯与酸分层。
A.水浴加热可保持温度恒定,水浴加热的优点为使反应物受热均匀、容易控制温度,A正确;
B.混合时先加浓硝酸,再加浓硫酸,最后加苯,因此混合时,应向浓硝酸中加入浓硫酸,待冷却至室温后,再将所得混合物加入苯中,B正确;
C.冷凝管可冷凝回流反应物,则仪器a的作用是冷凝回流,提高原料的利用率,C正确;
D.反应完全后,硝基苯与酸分层,应分液分离出有机物,再蒸馏分离出硝基苯,D错误;
故合理选项是D。

 阅读快车系列答案
阅读快车系列答案【题目】为了测定草酸晶体H2C2O4·xH2O中的x值,某实验小组进行实验,步骤如下:
①称取1.260g草酸晶体,配成100mL溶液。
②取25.00mL该H2C2O4溶液加入锥形瓶内,再加入适量稀硫酸。
③用浓度为0.1000mol/L的KMnO4溶液滴定H2C2O4溶液,当_________________时,滴定结束。
④记录数据,重复实验。整理数据如下:
实验序号 | V(KMnO4溶液) | |
滴定前刻度/mL | 滴定后刻度/mL | |
1 | 0.10 | 10.00 |
2 | 1.10 | 11.10 |
3 | 1.50 | 13.50 |
4 | 0.70 | 10.80 |
回答下列问题:
(1)步骤①需要使用烧杯、量筒、玻璃棒,还缺少的玻璃仪器为_______(填名称);步骤③滴定过程中,盛装KMnO4溶液的仪器为______(填名称)。
(2)该反应原理的化学方程式为_________________;
(3)请将步骤③补充完整__________________;
(4)根据数据,计算H2C2O4溶液的物质的量浓度为______________mol/L,x=____________;
(5)若滴定终点读数时俯视KMnO4溶液液面,则x值会__________(填“偏大”、“偏小”或“无影响”)。
【题目】已知25 ℃时有关弱酸的电离平衡常数见下表:
弱酸化学式 | HA | H2B |
电离平衡常数(25 ℃) | Ka=1.7×10-6 | Ka1=1.3×10-3 Ka2=5.6×10-8 |
则下列有关说法正确的是( )
A.NaHB溶液中部分微粒浓度的大小为:c(Na+)>c(HB-)>c(B2-)>c(H2B)
B.等物质的量浓度的各溶液pH关系为:pH(Na2B)>pH(NaHB)>pH(NaA)
C.向Na2B溶液中加入足量的HA溶液发生反应的离子方程式为:B2-+2HA=2A-+H2B
D.将a mol/L的HA溶液与a mol/L的NaA溶液等体积混合,混合液中:c(Na+)>c(A-)