题目内容
某溶液仅含Fe2+、Na+、Al3+、Ba2+、SO42-、NO3-、Cl-中的4种离子,所含离子的物质的量均为0.1mol。若向该溶液中加入过量的稀硫酸,有气体产生,且溶液中阴离子种类不变(不考虑水的电离和离子的水解)。回答下列问题:
(1)若向该溶液中加入过量的稀硫酸和KSCN溶液,现象是: ;
(2)写出向该溶液中加入过量的稀硫酸发生反应的离子方程式为:________________________________________________________________________;
(3)经分析,该溶液仅含的4种离子是:______________________________________;
(4)判定另外3种离子不能存在的主要依据有三个:
①向该溶液中加入过量的稀硫酸,有气体产生,且溶液中阴离子种类不变,②所含离子的物质的量均为0.1mol,则③是__________________________________________;
(5) 若向该溶液中加入足量的NaOH溶液,将所得的沉淀过滤再灼烧,最后所得固体的质量为______g
(1)若向该溶液中加入过量的稀硫酸和KSCN溶液,现象是: ;
(2)写出向该溶液中加入过量的稀硫酸发生反应的离子方程式为:________________________________________________________________________;
(3)经分析,该溶液仅含的4种离子是:______________________________________;
(4)判定另外3种离子不能存在的主要依据有三个:
①向该溶液中加入过量的稀硫酸,有气体产生,且溶液中阴离子种类不变,②所含离子的物质的量均为0.1mol,则③是__________________________________________;
(5) 若向该溶液中加入足量的NaOH溶液,将所得的沉淀过滤再灼烧,最后所得固体的质量为______g
(1)有气泡产生,溶液呈红色 ;
(2)3 Fe2+ + NO3- + 4 H+ =" 3" Fe3+ + NO↑ + 2 H2O ;
(3)Fe2+、SO42-、NO3-、Na+;
(4)溶液中离子的电荷守恒 ;
(5)8
(2)3 Fe2+ + NO3- + 4 H+ =" 3" Fe3+ + NO↑ + 2 H2O ;
(3)Fe2+、SO42-、NO3-、Na+;
(4)溶液中离子的电荷守恒 ;
(5)8
试题分析:由题意“若向该溶液中加入过量的稀硫酸,有气体产生,且溶液中阴离子种类不变”可知含有Fe2+、SO42-、NO3-;而且由于发生反应3 Fe2+ + NO3- + 4 H+ =" 3" Fe3+ + NO↑ + 2 H2O ;而产生气体,
又因为含有的离子的物质的量相等,由电荷守恒确定含有Na+;Fe2+的物质的量为0.1mol,“若向该溶液中加入足量的NaOH溶液,将所得的沉淀过滤再灼烧,”最后得到的固体为Fe2O3物质的量为0.05mol,质量为0.05mol×160g/mol=8g。

练习册系列答案
相关题目
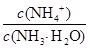 的值 (填“增大”、“减小”或“不变”)。
的值 (填“增大”、“减小”或“不变”)。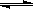 H++OH- KW=10-14 CH3COOH
H++OH- KW=10-14 CH3COOH 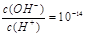 的溶液中存在Al3+、NH4+、Cl-、NO3-
的溶液中存在Al3+、NH4+、Cl-、NO3-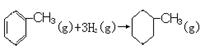 的焓变
的焓变