题目内容
6.碳及其化合物有广泛的用途.(1)反应C(s)+H2O(g)?CO(g)+H2(g);△H=+131.3kJ•mol-1,达到平衡后,体积不变时,以下有利于提高H2产率的措施是BC.
A.增加碳的用量
B.升高温度
C.用CO吸收剂除去CO
D.加入催化剂.
(2)已知,C(s)+CO2(g)?2CO(g);△H=+172.5kJ•mol-1,则反应 CO(g)+H2O(g)?CO2(g)+H2(g)的△H=-41.2kJ•mol-1.
(3)CO与H2一定条件下反应生成甲醇(CH3OH),甲醇是一种燃料,可利用甲醇设计一个燃料电池,用稀硫酸作电解质溶液,多孔石墨做电极,该电池负极反应式为CH3OH-6e-+H2O═CO2+6H+.
(4)在一定温度下,将CO(g)和H2O(g)各0.16mol分别通入到体积为2.0L的恒容密闭容器中,发生以下反应:CO(g)+H2O(g)?CO2(g)+H2(g),得到如下数据:
| t/min | 2 | 4 | 7 | 9 |
| n(H2O)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
②该温度下,此反应的平衡常数K=0.36.
③其他条件不变,再充入0.1mol CO和0.1mol H2O(g),平衡时CO的体积分数不变(填“增大”、“减小”或“不变”).
分析 (1)提高H2的产率,应改变条件使平衡正向移动,结合平衡移动原理分析解答;
(2)已知:①C(s)+H2O(g)?CO(g)+H2(g);△H=+131.3kJ•mol-1
②C(s)+CO2(g)?2CO(g);△H=+172.5kJ•mol-1
根据盖斯定律,①-②可得:CO(g)+H2O(g)?CO2(g)+H2(g);
(3)原电池负极发生氧化反应,甲醇在负极失去电子,酸性条件下生成二氧化碳,由电荷守恒可知还有氢离子生成;
(4)①由(2)中可知该反应为放热反应,降低温度平衡逆向移动,到达新平衡前正反应速率更大;
②7min到达平衡,平衡时水为0.1mol,则:
CO(g)+H2O(g)?CO2(g)+H2(g)
起始量(mol):0.16 0.16 0 0
变化量(mol):0.06 0.06 0.06 0.06
平衡量(mol):0.1 0.1 0.06 0.06
反应前后气体物质的量不变,用物质的量代替浓度代入K=$\frac{c(C{O}_{2})×c({H}_{2})}{c(CO)×c({H}_{2}O)}$计算平衡常数;
③其他条件不变,再充入0.1mol CO和0.1mol H2O(g),与原平衡中CO、H2O的起始物质的量之比均为1:1,反应前后气体体积不变,恒温恒容下为等效平衡,平衡时同种物质的含量相等.
解答 解:(1)①A.碳为固体,增加碳的用量不影响平衡移动,H2的产率不变,故A错误;
B.正反应为吸热反应反应,升高温度,平衡正向移动,H2的产率增大,故B正确;
C.用CO吸收剂除去CO,平衡正向移动,H2的产率增大,故C正确,
D.加入催化剂,可以加快反应速率,但不影响平衡移动,H2的产率不变,故D错误,
故选:BC;
(2)已知:①C(s)+H2O(g)?CO(g)+H2(g);△H=+131.3kJ•mol-1
②C(s)+CO2(g)?2CO(g);△H=+172.5kJ•mol-1
根据盖斯定律,①-②可得:CO(g)+H2O(g)?CO2(g)+H2(g),△H=131.3kJ•mol-1-131.3kJ•mol-1=-41.2kJ•mol-1,
故答案为:-41.2;
(3)原电池负极发生氧化反应,甲醇在负极失去电子,酸性条件下生成二氧化碳,由电荷守恒可知还有氢离子生成,负极电极反应式为:CH3OH-6e-+H2O═CO2+6H+,
故答案为:CH3OH-6e-+H2O═CO2+6H+;
(4)①由(2)中可知该反应为放热反应,降低温度平衡逆向移动,达到新平衡前v(逆)<v(正),
故答案为:<;
②7min到达平衡,平衡时水为0.1mol,则:
CO(g)+H2O(g)?CO2(g)+H2(g)
起始量(mol):0.16 0.16 0 0
变化量(mol):0.06 0.06 0.06 0.06
平衡量(mol):0.1 0.1 0.06 0.06
反应前后气体物质的量不变,可以用物质的量代替浓度计算平衡常数,则K=$\frac{c(C{O}_{2})×c({H}_{2})}{c(CO)×c({H}_{2}O)}$=$\frac{0.06×0.06}{0.1×0.1}$=0.36,
故答案为:0.36;
③其他条件不变,再充入0.1mol CO和0.1mol H2O(g),与原平衡中CO、H2O的起始物质的量之比均为1:1,反应前后气体体积不变,恒温恒容下为等效平衡,平衡时同种物质的含量相等,平衡时CO的体积分数不变,
故答案为:不变.
点评 本题考查化学平衡计算与影响因素、平衡常数、反应热计算、原电池等,(4)中③注意利用等效平衡分析解答,避免利用平衡常数计算解答的繁琐.

| A. | 干冰制冷 | B. | 高炉炼铁 | C. | 醋酸除垢 | D. | 纯碱去油 |
| A. | NH4F水溶液中含有HF,因此NH4F溶液不能存放于玻璃试剂瓶中 | |
| B. | 能使润湿的淀粉KI试纸变成蓝色的物质一定是Cl2 | |
| C. | 某溶液中加入CCl4,CC14层显紫色,证明原溶液中存在I- | |
| D. | 某溶液中加入BaCl2溶液,产生不溶于稀硝酸的白色沉淀,该溶液一定含有SO42- |
| A. | 称量10.6 g Na2CO3溶于100 mL水中 | |
| B. | 称量28.6 g Na2CO3•10H2O溶于少量水中,再用水稀释至100 mL | |
| C. | 量取20 mL 5.0 mol/L Na2CO3溶液用水稀释至100 mL | |
| D. | 配制80 mL 1.0 mol/L Na2CO3溶液,则只需要称量8.5 g Na2CO3 |
(1)工业冶炼铝,以石墨为阳极.阳极反应式为2O2--4e-=O2↑,可能发生副反应有C+O2$\frac{\underline{\;高温\;}}{\;}$CO2(或2C+O2$\frac{\underline{\;高温\;}}{\;}$2CO).
(2)一氧化碳和空气在酸性介质中构成燃料电池,负极反应式为CO-2e-+H2O=CO2+2H+
(3)向75mL 4mol•L-1KOH溶液中缓慢通入4480mL CO2气体(标准状况)恰好完全被吸收.
①写出该反应的离子方程式:2CO2+3OH-=CO32-+HCO3-+H2O.
②该吸收溶液中离子浓度大小排序为c(K+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+).
③常温下,a mol•L-1KHCO3溶液的pH=8,HCO3-的水解常数约等于$\frac{1{0}^{-12}}{a-1{0}^{-6}}$.(用含a式表示).
(4)已知:①2H2(g)+O2(g)═2H2O(l)△H1=-571.6kJ•mol-1
②2CO(g)+O2(g)═2CO2(g)△H2=-566.0kJ•mol-1
③CO(g)+2H2(g)?CH3OH(g)△H3=-90.8kJ•mol-1
计算甲醇蒸气的燃烧热△H=-763.8kJ•mol-1.
(5)某温度下,发生可逆反应:CO(g)+H2O(g)?CO2(g)+H2(g)△H=-41.0kJ•mol-1
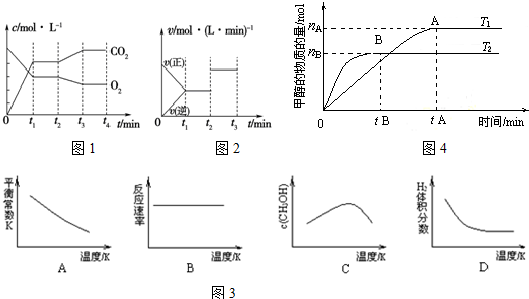
①向某容器中充入1.0mol H2O和1.0mol CO (g),在一定条件下发生上述反应.混合气体中CO的物质的量与时间关系如下列所示:
| 0 | 5min | 10min | 15min | 20min | 25min | |
| Ⅰ(800℃) | 1.0 | 0.80 | 0.70 | 0.65 | 0.50 | 0.50 |
| Ⅱ(800℃) | 1.0 | 0.7 | 0.60 | 0.50 | 0.50 | 0.50 |
②若开始向绝热容器中投入一定量二氧化碳、氢气在一定条件下发生上述可逆反应.
下列图象正确且说明可逆反应达到平衡状态的是A.(填序号)

(1)氮化硅(Si3N4)是一种新型陶瓷材料,它可由SiO2与过量焦炭在1300~1700°C的氮气流中反应制得:3SiO2(s)+6C(s)+2N2(g)?Si3N4(s)+6CO(g)△H=-1591.2kJ/mol,则该反应每转移1mole-,可放出的热量为132.6kJ.
(2)高温时,用CO还原MgSO4可制备高纯MgO.
①750℃时,测得气体中含等物质的量的SO2和SO3,此时反应的化学方程式是CO+2MgSO4 $\frac{\underline{\;高温\;}}{\;}$2MgO+CO2+SO2+SO3.
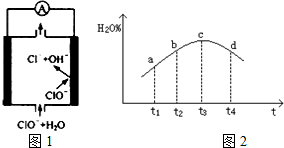
②由MgO制成的Mg可构成“镁-次氯酸盐”电池,其装置示意图如图1,该电池的正极反应式为ClO-+2e-+H2O=Cl-+2OH-.
(3)某研究小组将三组CO(g)与H2O(g)的混合气体分别通入体积为2L的恒容密闭容器中,一定条件下发生反应:CO(g)+H2O(g)?CO2(g)+H2(g),得到如下数据:
| 实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达平衡所需时间/min | ||
| CO | H2O | CO | H2 | |||
| 1 | 650 | 2 | 4 | 0.5 | 1.5 | 5 |
| 2 | 900 | 1 | 2 | 0.5 | 0.5 | - |
②下列能判断实验Ⅱ已经达到平衡状态的是(填写选项序号)ad.
a.容器内CO、H2O、CO2、H2的浓度不再变化 b.容器内压强不再变化
c.混合气体的密度保持不变 d.v正(CO)=v逆(CO2)
e.容器中气体的平均相对分子质量不随时间而变化
③若实验Ⅲ的容器是绝热的密闭容器,实验测得H2O(g)的转化率H2O%随时间变化的示意图如图2所示,b点v正>v逆(填“<”、“=”或“>”),t3~t4时刻,H2O(g)的转化率H2O%降低的原因是该反应达到平衡后,因反应为放热反应且反应容器为绝热容器,故容器内温度升高,反应逆向进行.