题目内容
现有A、B、C、D、E五种可溶强电解质,它们在水中可电离产生下列离子(各种离子不重复)。
已知:①A、B两溶液呈碱性; C、D、E溶液呈酸性。
②向E溶液中逐滴滴加B溶液至过量,沉淀量先增加后减少但不消失。
③D溶液与另外四种溶液反应都能产生沉淀。
试回答下列问题:
(1)A溶液呈碱性的原因是 (用离子方程式表示)。
(2)写出E溶液与过量的B溶液反应的离子方程式 。
(3)若25°时C、E溶液pH=4,则E溶液中水电离出的氢离子浓度是C溶液中水电离出的氢离子
浓度 倍。
(4)将C溶液逐滴加入等体积、等物质的量的浓度的A溶液中,反应后溶液中一价离子(+1或-1)
浓度由大到小的顺序为: 。
| 阳离子 | H+、Na+、Al3+、Ag+、Ba2+ |
| 阴离子 | OH-、Cl-、CO32-、NO3-、SO42- |
已知:①A、B两溶液呈碱性; C、D、E溶液呈酸性。
②向E溶液中逐滴滴加B溶液至过量,沉淀量先增加后减少但不消失。
③D溶液与另外四种溶液反应都能产生沉淀。
试回答下列问题:
(1)A溶液呈碱性的原因是 (用离子方程式表示)。
(2)写出E溶液与过量的B溶液反应的离子方程式 。
(3)若25°时C、E溶液pH=4,则E溶液中水电离出的氢离子浓度是C溶液中水电离出的氢离子
浓度 倍。
(4)将C溶液逐滴加入等体积、等物质的量的浓度的A溶液中,反应后溶液中一价离子(+1或-1)
浓度由大到小的顺序为: 。
(1)CO2-+H2O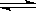 HCO3-+OH- (2分)
HCO3-+OH- (2分)
(2)3Ba2++8OH-+2Al3++3SO42-=3BaSO4↓+2AlO2-+4H2O (2分)
(3)106 (2分)
(4)c(Na+)>c(C1-)>c(HCO3-)>c(OH-)>c(H+)(2分)
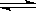 HCO3-+OH- (2分)
HCO3-+OH- (2分)(2)3Ba2++8OH-+2Al3++3SO42-=3BaSO4↓+2AlO2-+4H2O (2分)
(3)106 (2分)
(4)c(Na+)>c(C1-)>c(HCO3-)>c(OH-)>c(H+)(2分)
试题分析:(1)碳酸根水解产生氢氧根使溶液呈碱性:CO32﹣+H2O?HCO3﹣+OH﹣,故答案为:CO32﹣+H2O?HCO3﹣+OH﹣;(2)硫酸铝和过量的氢氧化钡反应,按照物质的量之比是1:4,方程式为:Al2(SO4)3+4Ba(OH)2═Ba(AlO2)2+3BaSO4↓+4H2O,离子方程式为:2Al3++3SO42﹣+3Ba2++8OH﹣═2AlO2﹣+4H2O+3BaSO4↓;(3)盐酸溶液的pH=4,则C(H+)=10﹣4 mol/L,则C(OH﹣)=
 =10﹣10 mol/L,OH﹣完全是由水电离产生,所以水电离出的氢离子浓度=10﹣10 mol/L;硫酸铝在溶液中水水解使水显示酸性,溶液中的氢离子浓度就是水电离出的氢离子浓度,PH=4,则C(H+)=10﹣4 mol/L,所以硫酸铝溶液中水电离出的氢离子浓度是盐酸溶液中水电离出的氢离子浓度的106倍,故答案为:106;(4)盐酸溶液逐滴加入等体积、等物质的量的浓度的碳酸钠溶液中,HCl与碳酸钠反应生成等物质的量的NaHCO3和NaCl,碳酸氢根离子的水解大于电离,溶液显碱性,所以离子浓度为:c(Na+)>c(C1﹣)>c(HCO3﹣)>c(OH﹣)>c(H+),故答案为:c(Na+)>c(C1﹣)>c(HCO3﹣)>c(OH﹣)>c(H+)。
=10﹣10 mol/L,OH﹣完全是由水电离产生,所以水电离出的氢离子浓度=10﹣10 mol/L;硫酸铝在溶液中水水解使水显示酸性,溶液中的氢离子浓度就是水电离出的氢离子浓度,PH=4,则C(H+)=10﹣4 mol/L,所以硫酸铝溶液中水电离出的氢离子浓度是盐酸溶液中水电离出的氢离子浓度的106倍,故答案为:106;(4)盐酸溶液逐滴加入等体积、等物质的量的浓度的碳酸钠溶液中,HCl与碳酸钠反应生成等物质的量的NaHCO3和NaCl,碳酸氢根离子的水解大于电离,溶液显碱性,所以离子浓度为:c(Na+)>c(C1﹣)>c(HCO3﹣)>c(OH﹣)>c(H+),故答案为:c(Na+)>c(C1﹣)>c(HCO3﹣)>c(OH﹣)>c(H+)。
练习册系列答案
相关题目
 。已知该溶液可与Al2O3反应,则:
。已知该溶液可与Al2O3反应,则: 生成,则原溶液中一定含有_______,可能含有大量的_______。
生成,则原溶液中一定含有_______,可能含有大量的_______。