题目内容
【题目】下到有关电解质溶液的说法不正确的是( )
A. 向Na2CO3溶液中通入NH3,  减小
减小
B. 将0.1mol·L-1的K2C2O4溶液从25℃升温至35℃, 增大
增大
C. 向0.1mol·L-1的HF溶液中滴加NaOH溶液至中性,  =1
=1
D. 向0.1mol·L-1的CH3COONa溶液中加入少量水, 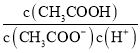 增大
增大
【答案】D
【解析】A项,Na2CO3溶液中存在平衡CO32-+H2O![]() HCO3-+OH-,通入NH3,NH3溶于水生成NH3H2O,存在电离NH3H2O
HCO3-+OH-,通入NH3,NH3溶于水生成NH3H2O,存在电离NH3H2O![]() NH4++OH-,抑制了CO32-的水解,c(CO32-)增大,又因为c(Na+)不变,所以
NH4++OH-,抑制了CO32-的水解,c(CO32-)增大,又因为c(Na+)不变,所以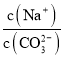 减小,故A正确;B项,K2C2O4溶液中存在C2O42-水解,水解吸热,若从25℃升温至35℃,促进了C2O42-的水解,c(C2O42-)减小,又因为c(Na+)不变,所以
减小,故A正确;B项,K2C2O4溶液中存在C2O42-水解,水解吸热,若从25℃升温至35℃,促进了C2O42-的水解,c(C2O42-)减小,又因为c(Na+)不变,所以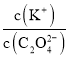 增大,故B正确;C项,向0.1mol·L-1的HF溶液中滴加NaOH溶液至中性,根据电荷守恒c(Na+)+c(H+)=c(F-)+c(OH-),c(H+)=c(OH-),则c(Na+)=c(F-),即
增大,故B正确;C项,向0.1mol·L-1的HF溶液中滴加NaOH溶液至中性,根据电荷守恒c(Na+)+c(H+)=c(F-)+c(OH-),c(H+)=c(OH-),则c(Na+)=c(F-),即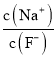 =1,故C正确;D项,CH3COOH的电离常数Ka=
=1,故C正确;D项,CH3COOH的电离常数Ka=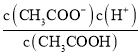 ,所以
,所以 =
=![]() ,电离常数只受温度影响,温度不变则Ka不变,故D错误。
,电离常数只受温度影响,温度不变则Ka不变,故D错误。

【题目】乙酰水杨酸(阿司匹林)是目前常用药物之一。实验室通过水杨酸进行乙酰化制备阿司匹林的一种方法如下:
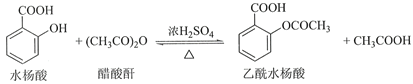
水杨酸 | 醋酸酐 | 乙酰水杨酸 | |
熔点/℃ | 157~159 | -72~-74 | 135~138 |
相对密度/(g·cm﹣3) | 1.44 | 1.10 | 1.35 |
相对分子质量 | 138 | 102 | 180 |
实验过程:在100 mL锥形瓶中加入水杨酸6.9 g及醋酸酐10 mL,充分摇动使固体完全溶解。缓慢滴加0.5 mL浓硫酸后加热,维持瓶内温度在70 ℃左右,充分反应。稍冷后进行如下操作.
①在不断搅拌下将反应后的混合物倒入100 mL冷水中,析出固体,过滤。
②所得结晶粗品加入50 mL饱和碳酸氢钠溶液,溶解、过滤。
③滤液用浓盐酸酸化后冷却、过滤得固体。
④固体经纯化得白色的乙酰水杨酸晶体5.4 g。
回答下列问题:
(1)该合成反应中应采用__________加热。(填标号)
A.热水浴 B.酒精灯 C.煤气灯 D.电炉
(2)下列玻璃仪器中,①中需使用的有________(填标号),不需使用的_______________________(填名称)。
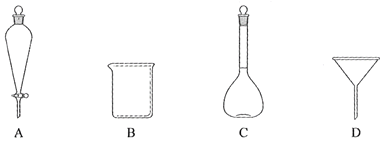
(3)①中需使用冷水,目的是______________________________________。
(4)②中饱和碳酸氢钠的作用是_________________________________,以便过滤除去难溶杂质。
(5)④采用的纯化方法为____________。
(6)本实验的产率是_________%。