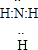题目内容
下列叙述正确的是
- A.浓硫酸的装运包装箱应贴上如图所示的标识

- B.用25ml酸式滴定管量取20.00ml 0.01 mol?L-1的Na2CO3溶液
- C.能使湿润的淀粉一碘化钾试纸变蓝的气体一定是Cl2
- D.从含I-的溶液中提取碘可以先加入稀硫酸与3%的H2O2溶液,再用酒精萃取
A
分析:A.根据浓硫酸具有强烈的腐蚀性,结合标志的含义进行分析判断;
B.碳酸钠是强碱弱酸盐,水解呈碱性;
C.湿润的KI淀粉试纸接触某气体而显蓝色,说明气体和碘离子反应把碘离子氧化为单质碘,遇到淀粉变蓝;
D.酒精和水相溶,所以不能用酒精萃取碘水中的碘.
解答:A.浓硫酸具有强烈的腐蚀性,故装运浓硫酸的包装箱应贴腐蚀品标志,图中所示标志是腐蚀品标志,故A正确;
B.酸式滴定管是磨口的玻璃活塞,玻璃的主要成分是二氧化硅,碳酸钠是强碱弱酸盐,水解溶液呈碱性,能与玻璃中二氧化硅反应,生成具有黏性的硅酸钠,导致玻璃塞打不开,所以用25ml酸式滴定管量取20.00ml 0.01 mol?L-1的Na2CO3溶液,酸式滴定管被碱腐蚀,故B错误;
C.溴单质溴蒸气可以把碘离子氧化为单质碘,碘单质遇到淀粉变蓝,NO2是强氧化性气体,可以把碘离子氧化为单质碘,碘单质遇到淀粉变蓝,所以能使湿润的淀粉一碘化钾试纸变蓝的气体不一定是Cl2,故C错误;
D.酒精和水是互溶的,不能做萃取剂来萃取点水中的碘单质,可以用四氯化碳来萃取,故D错误;
故选A.
点评:本题主要考查了实验操作,注意知识的积累,应注意积累实验操作中的易错点知识,题目难度不大.
分析:A.根据浓硫酸具有强烈的腐蚀性,结合标志的含义进行分析判断;
B.碳酸钠是强碱弱酸盐,水解呈碱性;
C.湿润的KI淀粉试纸接触某气体而显蓝色,说明气体和碘离子反应把碘离子氧化为单质碘,遇到淀粉变蓝;
D.酒精和水相溶,所以不能用酒精萃取碘水中的碘.
解答:A.浓硫酸具有强烈的腐蚀性,故装运浓硫酸的包装箱应贴腐蚀品标志,图中所示标志是腐蚀品标志,故A正确;
B.酸式滴定管是磨口的玻璃活塞,玻璃的主要成分是二氧化硅,碳酸钠是强碱弱酸盐,水解溶液呈碱性,能与玻璃中二氧化硅反应,生成具有黏性的硅酸钠,导致玻璃塞打不开,所以用25ml酸式滴定管量取20.00ml 0.01 mol?L-1的Na2CO3溶液,酸式滴定管被碱腐蚀,故B错误;
C.溴单质溴蒸气可以把碘离子氧化为单质碘,碘单质遇到淀粉变蓝,NO2是强氧化性气体,可以把碘离子氧化为单质碘,碘单质遇到淀粉变蓝,所以能使湿润的淀粉一碘化钾试纸变蓝的气体不一定是Cl2,故C错误;
D.酒精和水是互溶的,不能做萃取剂来萃取点水中的碘单质,可以用四氯化碳来萃取,故D错误;
故选A.
点评:本题主要考查了实验操作,注意知识的积累,应注意积累实验操作中的易错点知识,题目难度不大.

练习册系列答案
相关题目
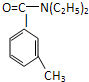 避蚊胺(又名DEET)是一种对人安全、活性高且无抗药性的新型驱蚊剂,其结构简式为:已知:RCOOH
避蚊胺(又名DEET)是一种对人安全、活性高且无抗药性的新型驱蚊剂,其结构简式为:已知:RCOOH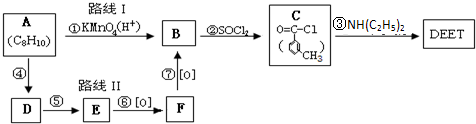


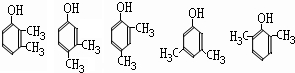 (任写2种)
(任写2种)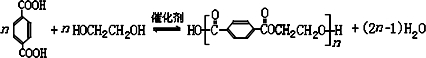

 NH3?H2O+H+
NH3?H2O+H+ (2010?崇文区二模)X、Y、Z、W均为含有10电子的微粒,其中X、Y、Z为分子,W为离子,且X与Z分子中含有的共用电子对数之比为3:4.
(2010?崇文区二模)X、Y、Z、W均为含有10电子的微粒,其中X、Y、Z为分子,W为离子,且X与Z分子中含有的共用电子对数之比为3:4.