题目内容
【题目】常温下向20mL0.1mol/LHA溶液中逐滴加入0.1mol/LNaOH溶液,其pH变化情况如图所示(忽略温度变化).下列说法中不正确的是( ) 
A.由题可知HA为弱酸
B.滴定终点位于c和d点之间
C.滴定到b点时:n(Na+)+n(H+)﹣n(OH﹣)+n(HA)=0.002mol
D.滴定到d点时:c(OH﹣)>c(Na+)>c(A﹣)>c(H+)
【答案】B
【解析】解:A、20mL0.1mol/LHA溶液pH=3,所以酸是弱酸,故A正确;B、向20mL0.1mol/LHA溶液中逐滴加入0.1mol/LNaOH溶液,恰好中和时溶液呈碱性,pH>7,溶液呈中性,需要酸稍过量,滴定终点位于c和b点之间,故B错误;
C、滴定到b点时,根据电荷守恒:n(Na+)+n(H+)﹣n(OH﹣)=n(A﹣),n(A﹣)+n(HA)=0.002mol,即n(Na+)+n(H+)﹣n(OH﹣)+n(HA)=0.002mol,故C正确;
D、d点所的溶液是氢氧化钠和醋酸钠溶液的混合物,所以c(Na+)>c(A﹣),氢氧化钠剩余,c(Na+)>c(OH﹣)>c(A﹣)>c(H+),故D正确,
故选B.

【题目】C、N、O、Al、Si、Cu是常见的六种元素.
(1)Si位于元索周期表第周期第族.
(2)N原子的原子结构示意图为;Cu的低价氧化物的颜色为 .
(3)用“>”或“<”填空:
原子半径 | 电负性 | 熔点 | 沸点 |
AlSi | NO | 金刚石晶体硅 | CH4SiH4 |
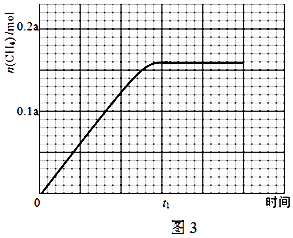
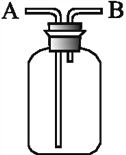
(4)常温下,将除去表面氧化膜的Al、Cu片插入浓HNO3中组成原电池(图1),测得原电池的电流强度(I)随时间(t)的变化如图2所示,反应过程中有红棕色气体产生. 
0﹣t1时,原电池的负极是Al片,此时,正极的电极反应式是 , 溶液中的H+向极移动,t1时,原电池中电子流动方向发生改变,其原因是 .