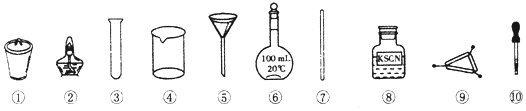
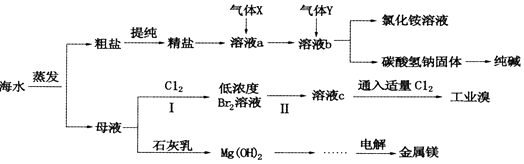
��Ŀ����
����Ŀ��FeCl3���ִ���ҵ������Ӧ�ù㷺��ij��ѧ�о���ѧϰС��ģ�ҵ�����Ʊ���ˮFeCl3�����ø���ƷFeCl3��Һ�����ж���H2S���塣
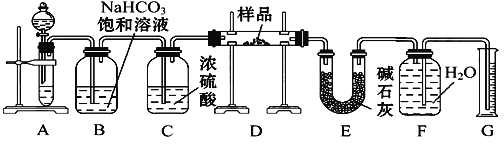
��.���������ϵ�֪����ˮFeCl3�ڿ������׳��⣬������������������Ϊ���ᡣ����������Ʊ���ˮFeCl3��ʵ�鷽����װ��ʾ��ͼ(���ȼ��г�װ����ȥ)�������������£�

�ټ���װ�õ������ԣ�
��ͨ������Cl2���Ͼ�װ���еĿ�����
���þƾ�������м�·���������Ӧ��ɣ�
�ܡ���
����ϵ��ȴ��ֹͣͨ��Cl2�����ø����N2�Ͼ�Cl2�����ռ����ܷ⡣
��ش��������⣺
��1��װ��A�з�Ӧ�Ļ�ѧ����ʽΪ_______________________________________��
��2���ڢ۲����Ⱥ����ɵ���״FeCl3�ֽ����ռ��������������ڷ�Ӧ��A�Ҷˡ�Ҫʹ������FeCl3�����ռ������ڢܲ�����Ӧ����__________________________________��
��3�����������У�Ϊ��ֹFeCl3��������ȡ�Ĵ�ʩ��(������)____________��
��4��װ��B����ˮԡ������Ϊ_______________________________________________��װ��C������Ϊ________��װ��D��FeCl2ȫ����Ӧ����ʧȥ����Cl2�����ö�ʧЧ��д������FeCl2�Ƿ�ʧЧ���Լ�_______________________________________________��
��5�������߿��л���β������װ��E��ע���Լ������ڴ���ϻ���____________
��6��FeCl3��Һ��H2S���巴Ӧ�����ӷ���ʽΪ____________________________��
���𰸡� ![]() �ڳ�����FeCl3�����·����� �ڢ� ��ȴFeCl3ʹ������������ռ���Ʒ ����� K3[Fe(CN)6]��Һ�����Ը��������Һ
�ڳ�����FeCl3�����·����� �ڢ� ��ȴFeCl3ʹ������������ռ���Ʒ ����� K3[Fe(CN)6]��Һ�����Ը��������Һ 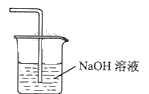
![]()
����������1��װ��A������������Ӧ�����Ȼ�������ӦΪ2Fe+3Cl2 ![]() 2FeCl3����2����FeCl3���ȷ�������ʹ������FeCl3�����ռ������ʴ�Ϊ���ڳ�����FeCl3�����·����ȣ���3��Ϊ��ֹFeCl3��������ȡ�Ĵ�ʩ�Т�ͨ������Cl2���ø����N2�Ͼ�Cl2����ѡ���ڢ�����4��B�е���ˮ����Ϊ����ȴFeCl3ʹ������������ռ���Ʒ��װ��C������Ϊ����ܣ�����FeCl2�Ƿ�ʧЧӦ����FeCl2�Ƿ���ڣ�������KMnO4��Һ��K3[Fe(CN)6]��Һ���飻��5��������������Һ���յ������������ÿ��Ƿ��������ʴ�Ϊ��
2FeCl3����2����FeCl3���ȷ�������ʹ������FeCl3�����ռ������ʴ�Ϊ���ڳ�����FeCl3�����·����ȣ���3��Ϊ��ֹFeCl3��������ȡ�Ĵ�ʩ�Т�ͨ������Cl2���ø����N2�Ͼ�Cl2����ѡ���ڢ�����4��B�е���ˮ����Ϊ����ȴFeCl3ʹ������������ռ���Ʒ��װ��C������Ϊ����ܣ�����FeCl2�Ƿ�ʧЧӦ����FeCl2�Ƿ���ڣ�������KMnO4��Һ��K3[Fe(CN)6]��Һ���飻��5��������������Һ���յ������������ÿ��Ƿ��������ʴ�Ϊ��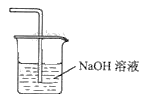 ����6�����������������ԣ�������л�ԭ�ԣ�����֮�䷢��������ԭ��Ӧ��2FeCl3+3H2S=2FeCl2+6HCl+3S�������ӷ���ʽΪ��2Fe3++H2S=2Fe2++S��+2H+��
����6�����������������ԣ�������л�ԭ�ԣ�����֮�䷢��������ԭ��Ӧ��2FeCl3+3H2S=2FeCl2+6HCl+3S�������ӷ���ʽΪ��2Fe3++H2S=2Fe2++S��+2H+��

 ����ѧҵ���Ե�����ϵ�д�
����ѧҵ���Ե�����ϵ�д�