题目内容
19.某固体化合物R不导电,熔化或溶于水都能导电,有关R的叙述正确的是( )| A. | R一定是一种盐 | B. | R一定是一种强碱 | ||
| C. | R一定是离子化合物 | D. | R可能是强酸 |
分析 固体化合物R不导电,熔化或溶于水都能导电,则R中存在离子,一定为离子化合物,以此来解答.
解答 解:由信息可知,化合物熔化能导电,则一定含离子,
A.R可能为金属氧化物,不一定属于盐,故A错误;
B.R可能为盐,如NaCl,不一定属于强碱,故B错误;
C.由上述分析可知,一定为离子化合物,故C正确;
D.R不可能为强酸,强酸为共价化合物,故D错误;
故选C.
点评 本题考查酸碱盐及离子化合物的关系,为基础性习题,把握习题中的信息化合物熔化导电为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案
相关题目
7.常温下,把1mL 0.1mol/L的硫酸加水稀释制成2L溶液,在此溶液中由水电离产生的H+,接近于( )
| A. | 1.0×10-4 mol/L | B. | 1.0×10-8 mol/L | ||
| C. | 1.0×10-11 mol/L | D. | 1.0×10-10 mol/L |
14.将标准状况下3.36L HCl溶于水配成25mL溶液,现用此盐酸与19.5g锌粒反应制取氢气.试计算:(写出计算过程)
(1)此盐酸的物质的量浓度;
(2)若要使锌完全反应,则所需盐酸的最小体积.
(1)此盐酸的物质的量浓度;
(2)若要使锌完全反应,则所需盐酸的最小体积.
8.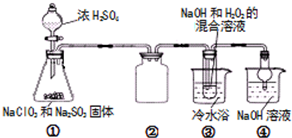 亚氯酸钠(NaClO2)是一种高效氧化剂、漂白剂.已知 NaClO2饱和溶液在温度低于38℃时析出的晶体是NaClO2•3H2O,高于38℃时析出固体是无水NaClO2,高于60℃时NaClO2分解成NaClO3和NaCl.利用下图所示装置制备亚氯酸钠.
亚氯酸钠(NaClO2)是一种高效氧化剂、漂白剂.已知 NaClO2饱和溶液在温度低于38℃时析出的晶体是NaClO2•3H2O,高于38℃时析出固体是无水NaClO2,高于60℃时NaClO2分解成NaClO3和NaCl.利用下图所示装置制备亚氯酸钠.
完成下列填空:
(1)组装好仪器后,检查装置气密性的操作是关闭分液漏斗的玻璃旋塞,将干燥管的末端浸末在水中,微热锥形瓶,干燥管末端有气泡产生,停止加热一段时间后,有回流的液柱,则气密性良好.
(2)装置①中用NaClO3、Na2SO3和浓H2SO4反应制得ClO2,写出该反应的化学方程式2NaClO3+Na2SO3+H2SO4(浓)=2ClO2↑+2Na2SO4+H2O,装置③发生反应的离子方程式为2ClO2+H2O2+2Na++2OH-+4H2O=2NaClO2•3H2O+O2↑.
(3)装置③反应后的溶液中还含有少量NaOH杂质,从该溶液获得无水NaClO2晶体的操作步骤为:
①50℃左右蒸发结晶;
②趁热过滤;
③用50℃左右的温水洗涤;
④低于60℃干燥,得到成品.
步骤③中用50℃左右的温水洗涤的原因是防止产生NaClO2•3H2O晶体.
(4)①准确称取所得亚氯酸钠样品10.0g于烧杯中,加入适量蒸馏水和过量的碘化钾晶体,再滴入适量的稀硫酸,充分反应.将所得混合液配成250mL待测溶液.
②取25.00mL待测液,用2.0mol•L-1Na2S2O3标准液滴定(I2+2S2O32-→2I-+S4O62-),以淀粉溶液做指示剂,达到滴定终点时的现象为当滴入最后一滴Na2S2O3时,溶液由蓝色变为无色且半分钟内不变色.重复滴定3次,测得数据如表所示,则该样品中NaClO2的质量分数为90.5%.
(5)在实验过程中,下列操作会使实验结果偏高的是a、d
a.读取标准液体积时,开始时平视读数,结束时仰视读数
b.配制250mL待测液时,定容后摇匀发现液面下降,又补加水重新达到刻度线
c.盛装待测液的滴定管注液前未用待测溶液润洗
d.盛装标准液的滴定管尖嘴处滴定前有气泡,滴定终点时气泡消失
(6)已知常温下Ka(HClO2)=1×10-2、Ka(CH3COOH)=1.75×10-5,则0.1mol/L的HClO2溶液与0.05mol/L的NaOH溶液等体积混合所得溶液中各离子浓度由大到小的顺序为c(ClO2-)>c(Na+)>c(H+)>c(OH-).
 亚氯酸钠(NaClO2)是一种高效氧化剂、漂白剂.已知 NaClO2饱和溶液在温度低于38℃时析出的晶体是NaClO2•3H2O,高于38℃时析出固体是无水NaClO2,高于60℃时NaClO2分解成NaClO3和NaCl.利用下图所示装置制备亚氯酸钠.
亚氯酸钠(NaClO2)是一种高效氧化剂、漂白剂.已知 NaClO2饱和溶液在温度低于38℃时析出的晶体是NaClO2•3H2O,高于38℃时析出固体是无水NaClO2,高于60℃时NaClO2分解成NaClO3和NaCl.利用下图所示装置制备亚氯酸钠.完成下列填空:
(1)组装好仪器后,检查装置气密性的操作是关闭分液漏斗的玻璃旋塞,将干燥管的末端浸末在水中,微热锥形瓶,干燥管末端有气泡产生,停止加热一段时间后,有回流的液柱,则气密性良好.
(2)装置①中用NaClO3、Na2SO3和浓H2SO4反应制得ClO2,写出该反应的化学方程式2NaClO3+Na2SO3+H2SO4(浓)=2ClO2↑+2Na2SO4+H2O,装置③发生反应的离子方程式为2ClO2+H2O2+2Na++2OH-+4H2O=2NaClO2•3H2O+O2↑.
(3)装置③反应后的溶液中还含有少量NaOH杂质,从该溶液获得无水NaClO2晶体的操作步骤为:
①50℃左右蒸发结晶;
②趁热过滤;
③用50℃左右的温水洗涤;
④低于60℃干燥,得到成品.
步骤③中用50℃左右的温水洗涤的原因是防止产生NaClO2•3H2O晶体.
| 实验序号 | 滴定前读数/mL | 滴定后读数/mL |
| 1 | 0.00 | 19.96 |
| 2 | 3.26 | 23.30 |
| 3 | 1.10 | 23.40 |
②取25.00mL待测液,用2.0mol•L-1Na2S2O3标准液滴定(I2+2S2O32-→2I-+S4O62-),以淀粉溶液做指示剂,达到滴定终点时的现象为当滴入最后一滴Na2S2O3时,溶液由蓝色变为无色且半分钟内不变色.重复滴定3次,测得数据如表所示,则该样品中NaClO2的质量分数为90.5%.
(5)在实验过程中,下列操作会使实验结果偏高的是a、d
a.读取标准液体积时,开始时平视读数,结束时仰视读数
b.配制250mL待测液时,定容后摇匀发现液面下降,又补加水重新达到刻度线
c.盛装待测液的滴定管注液前未用待测溶液润洗
d.盛装标准液的滴定管尖嘴处滴定前有气泡,滴定终点时气泡消失
(6)已知常温下Ka(HClO2)=1×10-2、Ka(CH3COOH)=1.75×10-5,则0.1mol/L的HClO2溶液与0.05mol/L的NaOH溶液等体积混合所得溶液中各离子浓度由大到小的顺序为c(ClO2-)>c(Na+)>c(H+)>c(OH-).
5.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 2.0gH218O与D2O的混合物中所含中子数为NA | |
| B. | 28 g乙烯(C2H4)和环丁烷(C4H8)的混合气体中含有的碳原子数为NA | |
| C. | 标准状况下,5.6LCO2与足量Na2O2反应转移的电子数为0.5 NA | |
| D. | 50ml 12mol/L盐酸与足量MnO2共热,转移的电子数为0.3NA |
6.设NA为阿伏伽德罗常数的值,下列叙述一定正确的是( )
| A. | 1 L 2 mol•L-1的NH4Cl溶液中含有的NH4+数目为2NA | |
| B. | 标况下,0.1mol苯中含有C=C键数目为0.3NA | |
| C. | 常温常压下,5.2g乙炔和苯的混合气体中含有的碳原子数为0.4NA | |
| D. | 7.8g过氧化钠与足量CO2反应,转移电子数为0.2NA,CO2为还原剂 |
