题目内容
小苏打、胃舒平、达喜都是常用的中和胃酸的药物。
(1)小苏打每片含0.50gNaHCO3,2片小苏打片和胃酸完全中和,被中和的H+是 mol。
(2)胃舒平每片含0.245gAl(OH)3,中和胃酸时,6片小苏打相当于胃舒平 片。
(3)达喜的化学成分是铝和镁的碱式盐:取该碱式盐3.01g,加入2.0mol/L盐酸使其溶解,当加入盐酸42.5mL时开始产生CO2,加入盐酸至45.0mL时正好完全反应,计算该碱式盐样品中氢氧根与碳酸根的物质的量之比 。
(1)0.012(2分) (2)3.8(2分) (3)16:1(2分)
解析试题分析:(1)2片小苏打所含NaHCO3的质量为0.50g×2=1.0g,其物质的量为1.0g÷84g/mol=0.012mol,
由HCO3-+H+=CO2↑+H2O,可知被中和的H+是n(H+)=0.012mol。
(2)6片小苏打的物质的量为0.012mol×3=0.036mol,即中和的H+为0.036mol,而每片的Al(OH)3的物质的量为0.245g÷78g/mol=0.0031mol,由Al(OH)3+3H+=Al3++3H2O可知,Al(OH)3的片数为:0.036mol÷0.0031mol÷3=3.8片。
(3)碱式盐中加入HCl,首先是碱式盐中的OH-和CO32-与H+(42.5mL)反应生成H2O和HCO3—,然后HCO3—继续与盐酸反应,消耗45.0mL时正好反应完全。所以n(HCO3-)=2.0mol?L-1×(0.045L—0.0425L)=0.005mol,即n(CO32-)=0.005mol,H+与CO32-、OH-反应的H+的总物质的量为:2.0mol?L-1×0.0425L=0.085mol,所以n(OH-)=0.08mol,该碱式盐样品中氢氧根与碳酸根的物质的量之比为16∶1。
考点:考查碳酸盐以及氢氧化铝与盐酸反应的有关计算

含有硫的化合物在工业生产中应用广泛,回答下列问题:
(1)黄铜矿是工业炼铜的主要原料,其主要成分为CuFeS2。
①测得某黄铜矿(CuFeS2)中含硫20%(质量分数),求该矿石含铜的质量分数。
②现有一种天然黄铜矿(含少量脉石),为了测定该黄铜矿的纯度,某同学设计了如下实验:称取
研细的黄铜矿样品1.150g,在空气中进行煅烧,生成Cu、Fe3O4和SO2气体,用100 mL滴有淀粉的
蒸馏水全部吸收SO2,然后取10mL吸收液,用0.05mol/L标准碘溶液进行滴定,用去标准碘溶液的体
积为20.00mL。求该黄铜矿的纯度。
(2)将FeS和Fe2O3的混和物56.6 g,用足量稀H2SO4溶解后可得3.2 g硫,原混和物中FeS的质量。
(3)一定温度下,硫酸铜受热分解生成CuO、SO2、SO3和O2。已知:SO2、SO3都能被碱石灰和氢氧
化钠溶液吸收。利用下图装置加热无水硫酸铜粉末直至完全分解。若无水硫酸铜粉末质量为10.0 g,
完全分解后,各装置的质量变化关系如下表所示。
| 装置 | A(试管+粉末) | B | C |
| 反应前 | 42.0 g | 75.0 g | 140.0 g |
| 反应后 | 37.0 g | 79.0 g | 140.5 g |
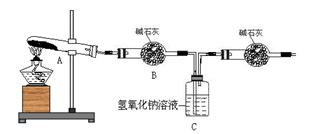
请通过计算,推断出该实验条件下硫酸铜分解的化学方程式。
(4)硫化钠是用于皮革的重要化学试剂,可用无水Na2SO4与炭粉在高温下反应制得,化学方程式如下:
①Na2SO4 + 4C
 Na2S + 4CO↑ ②Na2SO4 + 4CO
Na2S + 4CO↑ ②Na2SO4 + 4CO Na2S + 4CO2
Na2S + 4CO2 a.若在反应过程中,产生CO和CO2混合气体为2mol,求生成Na2S的物质的量。
b.硫化钠晶体放置在空气中,会缓慢氧化成Na2SO3,甚至是Na2SO4,现将43.72g部分变质的硫化钠样品溶于水中,加入足量盐酸后,过滤得4.8g沉淀和1.12L H2S 气体(标准状况,假设溶液中气体全部逸出),在滤液中加入足量的BaCl2后过滤得2.33g沉淀,分析该硫化钠样品的成分及其物质的量。
现有两份铵盐样品A、B,其成分都是(NH4)2SO4、NH4HSO4的混合物。甲、乙两个研究性学习小组的同学想要确定A和B中各成分的含量。
甲组同学取了数分相同质量的样品A溶于水,然后分别加入不同体积的1mol/L的NaOH溶液,水浴加热至气体全部逸出。(此温度下,铵盐不分解)。该气体干燥后用足量的浓硫酸完全吸收。浓硫酸增重的质量与加入NaOH溶液的体积的关系如图。分析该图像,并回答下列问题: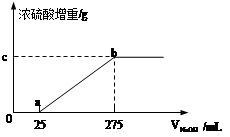
(1)写出ab段涉及的离子方程式: 。
(2)c点对应的数值是 ;样品A中(NH4)2SO4、NH4HSO4的物质的量之比为 。乙组同学取了数份不同质量的样品B,分别加入到200mL 1mol/L的NaOH溶液中,同样用水浴加热,将逸出气体干燥后再用浓H2SO4吸收。测定结果如下表:
| 实验编号 | Ⅰ | Ⅱ | Ⅲ | Ⅳ |
| 铵盐的质量(g) | 9.88 | 19.76 | 29.64 | 49.40 |
| 浓硫酸增加的质量(g) | m | m | 1.36 | 0 |
分析该表,并回答下列问题:
(3)①分析实验数据可知,实验编号为 的实验中,氢氧化钠足量,铵盐中的铵根离
子完全转化成气体;m的值为 。
②计算样品B中氮元素的质量分数。(用小数表示,保留两位小数)
(1)乙组同学在研究时发现,浓硫酸增重的质量与样品B的质量之间满足一定的函数关系。假设样品的质量为x(g),浓硫酸增重的质量为y(g)。求:当x在不同范围时y与x的函数关系。
淀粉和纤维素都可以用(C6H10O5)n表示分子组成,它们是
| A.同分异构体 | B.同一种物质 | C.同系物 | D.多糖类物质 |