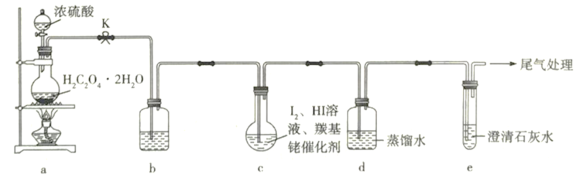
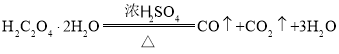题目内容
【题目】市售浓硫酸中溶质的质量分数为98%,密度为1.84 g·cm-3。计算市售浓硫酸中H2SO4的物质的量浓度_________。
【答案】18.4 mol·L-1
【解析】
根据题意可以计算出1000 mL浓硫酸中H2SO4的质量,然后将其换算成H2SO4的物质的量。
解法一:1000 mL浓硫酸中H2SO4的质量为m(H2SO4)=ρ[H2SO4(aq)]·V[H2SO4(aq)]·w(H2SO4)=1.84 g·cm-3×1 000 mL×98%=1 803.2 g,1 803.2 g H2SO4的物质的量为n(H2SO4)=![]() =
=![]() =18.4 mol;因为1 000 mL浓硫酸中含18.4 mol H2SO4,所以市售浓硫酸中H2SO4的物质的量浓度为18.4 mol·L-1。
=18.4 mol;因为1 000 mL浓硫酸中含18.4 mol H2SO4,所以市售浓硫酸中H2SO4的物质的量浓度为18.4 mol·L-1。
解法二 直接用公式c=![]() 来计算,c(H2SO4)=
来计算,c(H2SO4)=![]() =18.4 mol·L-1。
=18.4 mol·L-1。
答案:18.4 mol·L-1。

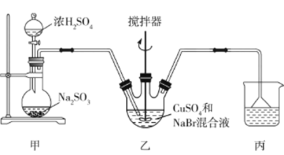
【题目】下列实验中,现象及得出的结论正确的是()
实验 | 现象 | 结论 | |
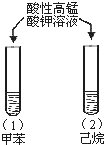
A |
| 试管(1)中紫色褪去, 试管(2)中紫色未褪 | 甲基使苯环的活性增强 |
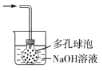
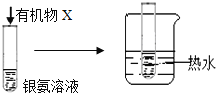
B |
| 试管内壁有 银镜生成 | 有机物X中一定含有醛基 |
C | 向淀粉溶液中加入稀硫酸,水浴加热,一段时间后,再加入新制的氢氧化铜悬浊液并加热 | 未见砖红色沉淀 | 淀粉未水解 |
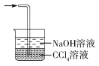
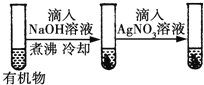
D |
| 最后一只试管中有浅黄色沉淀 | 有机物中含有溴原子 |
A.AB.BC.CD.D
【题目】工业上用软锰矿及含锰废料(主要成分![]() ,含有少量
,含有少量![]() 等)与烟气脱硫进行联合处理并制备
等)与烟气脱硫进行联合处理并制备![]() 的流程如下:
的流程如下:
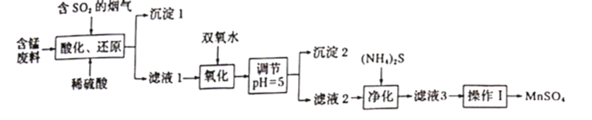
25℃时,几种金属离子沉淀时的pH如下:
|
|
|
|
| |
开始沉淀时pH | 7.6 | 2.7 | 3.8 | 8.3 | 5.9 |
完全沉淀时pH | 9.7 | 4.0 | 4.7 | 9.8 | 6.9 |
(1)![]() 在酸化还原步骤中所发生反应的离子方程式分别为_____________、_____________。
在酸化还原步骤中所发生反应的离子方程式分别为_____________、_____________。
(2)沉淀1为_________(填化学式),用双氧水处理滤液1时,通常在40~55℃下进行原因是_____________。
(3)氧化反应过程中常会有一定量的气泡产生,可能的原因是___________,调节溶液![]() 的目的是_______________
的目的是_______________
(4)“净化”时,加入![]() 的作用是______________
的作用是______________
(5)滤液3中除![]() 外,还含有少量
外,还含有少量![]() 。
。![]() 的溶解度曲线如图所示。据此判断,“操作I”应为___________、______、洗涤、干燥。
的溶解度曲线如图所示。据此判断,“操作I”应为___________、______、洗涤、干燥。