题目内容
8.已知NH4HCO3$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+CO2↑+H2O↑.为了将混有硫酸钠、碳酸氢铵的NaCl提纯,并制得纯净的NaCl溶液,某学生设计如下实验方案如图1:(1)操作①中盛放药品可选用坩埚 (填仪器名称),在加热过程中应不断搅拌 (填操作名称).
(2)操作③为什么不用硝酸钡溶液,其理由是会引入杂质硝酸根离子.
(3)进行操作③后,如何判断SQUOTE已除尽,方法是干净试管取上层清液少许于试管中,向此试管中滴加BaCl2溶液,若无沉淀,说明SO42-已除尽.
(4)操作④发生反应的化学方程式BaCl2+Na2CO3═BaCO3↓+2NaCl.
(5)说明此设计方案不严密之处及正确的方法在操作③时加入的Na2CO3溶液煮沸并不能除去,因此在操作④之后应加过量盐酸以除去Na2CO3,然后再加热煮沸除去HCl和CO2.
(6)若将纯净的NaCl溶液得到纯净的NaCl固体,还需的操作为蒸发、干燥.
(7)某研究小组同学得到另一份0.2L粗盐样品溶液,其相关信息如图2,请回答下列问题:
①该混合液中,NaCl的物质的量为0.2 mol,含溶质MgCl2的质量为9.5 g.
②该混合液中CaCl2的物质的量为0.1 mol,将该混合液加水稀释至体积为1L,稀释后溶液中Ca2+的物质的量浓度为0.1 mol•L-1.
③向该稀释后的溶液中加入足量硝酸酸化的硝酸银溶液,可得到沉淀0.6 mol.
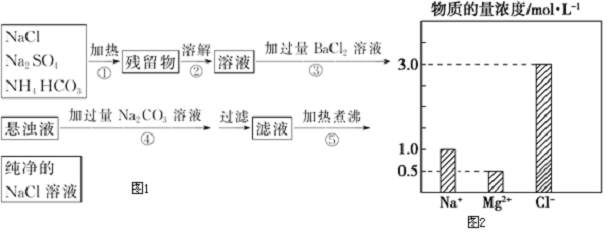
分析 混有硫酸钠、碳酸氢铵的氯化钠固体,由流程可知,①中发生加热条件下分解反应,分解后的固体溶于水后,与氯化钡反应除去硫酸根离子,再利用碳酸钠除去过量的钡离子,过滤后滤液中含NaCl、碳酸钠,加盐酸除去碳酸钠后溶质为NaCl,蒸发得到纯净的NaCl,以此解答(1)~(6);
(7)①由图可知,c(Na+)=1.0mol/L,c(Mg2+)=0.5mol/L,结合n=cV、m=nM计算;
②结合电荷守恒计算c(Ca2+),结合n=cV、c=$\frac{n}{V}$计算;
③加入足量硝酸酸化的硝酸银溶液,氯离子转化为AgCl沉淀.
解答 解:混有硫酸钠、碳酸氢铵的氯化钠固体,由流程可知,①中发生加热条件下分解反应,分解后的固体溶于水后,与氯化钡反应除去硫酸根离子,再利用碳酸钠除去过量的钡离子,过滤后滤液中含NaCl、碳酸钠,加盐酸除去碳酸钠后溶质为NaCl,蒸发得到纯净的NaCl,
(1)操作①为加热,盛放药品可选用坩埚,在加热过程中应不断搅拌,加快速率,故答案为:坩埚;搅拌;
(2)用硝酸钡溶液会引入杂质硝酸根离子,难以除去,故答案为:会引入杂质硝酸根离子;
(3)进行操作③后,判断溶液中SO42-已除尽的方法为取③反应后的上层清液再滴加氯化钡,若不生成沉淀,可除尽,
故答案为:用干净试管取上层清液少许于试管中,向此试管中滴加BaCl2溶液,若无沉淀,说明SO42-已除尽;
(4)操作④发生反应的化学方程式为BaCl2+Na2CO3═BaCO3↓+2NaCl,故答案为:BaCl2+Na2CO3═BaCO3↓+2NaCl;
(5)由上述分析可知,此设计方案不严密之处及正确的方法为在操作③时加入的Na2CO3溶液煮沸并不能除去,因此在操作④之后应加过量盐酸以除去Na2CO3,然后再加热煮沸除去HCl和CO2,故答案为:在操作③时加入的Na2CO3溶液煮沸并不能除去,因此在操作④之后应加过量盐酸以除去Na2CO3,然后再加热煮沸除去HCl和CO2;
(6)溶液得到纯净的NaCl固体,需要蒸发、干燥操作,故答案为:蒸发、干燥;
(7)①由图可知,c(Na+)=1.0mol/L,该混合液中,NaCl的物质的量为0.2L×1.0mol/L=0.2mol;c(Mg2+)=0.5mol/L,含溶质MgCl2的质量为0.2L×0.5mol/L×95g/mol=9.5g,故答案为:0.2;9.5;
②由电荷守恒可知2c(Ca2+)+c(Na+)+2c(Mg2+)=c(Cl-),解得c(Ca2+)=$\frac{3.0-1.0-0.5×2}{2}$=0.5mol/L,混合液中CaCl2的物质的量为0.2L×0.5mol/L=0.1mol,该混合液加水稀释至体积为1L,稀释后溶液中Ca2+的物质的量浓度为c=$\frac{n}{V}$=$\frac{0.1mol}{1L}$=0.1mol/L,故答案为:0.1;0.1;
③加入足量硝酸酸化的硝酸银溶液,氯离子转化为AgCl沉淀,n(AgCl)=n(Cl-)=3mol/L×0.2L=0.6mol,故答案为:0.6.
点评 本题考查混合物分离提纯实验方案的设计及计算,为高频考点,把握流程中的化学反应及混合物分离方法为解答的关键,侧重分析与实验能力、推断能力的考查,题目难度不大.

 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案 ABC考王全优卷系列答案
ABC考王全优卷系列答案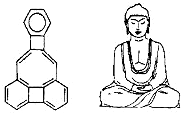 美国康乃尔大学的魏考克斯(C.Wilcox)所合成的一种有机分子,就像一尊释迦牟尼佛,因而称为释迦牟尼分子(所有原子在同一平面),有关该有机分子的说法正确的是( )
美国康乃尔大学的魏考克斯(C.Wilcox)所合成的一种有机分子,就像一尊释迦牟尼佛,因而称为释迦牟尼分子(所有原子在同一平面),有关该有机分子的说法正确的是( )| A. | 该有机物属于烃的衍生物 | B. | 该有机物属于苯的同系物 | ||
| C. | 该有机物分子中含有22个碳原子 | D. | 该有机物一氯代物只有4种 |
| A. | 丙酸遇紫色石蕊试剂变红 | B. | 丙酸与乙醇的酯化反应是取代反应 | ||
| C. | 丙酸和乙酸属于同一类物质 | D. | 丙酸可以和乙烯一样发生加成反应 |
| A. | 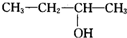 | B. | (CH3)3CCH2OH | C. | 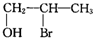 | D. | 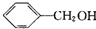 |
| A. | 碳酸钙溶于稀盐酸中:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| B. | 稀盐酸与铁粉反应:2Fe+6H+═2Fe3++3H2↑ | |
| C. | 把铜片放入硝酸银溶液中:Cu+Ag+═Cu2++Ag | |
| D. | 氢氧化钡溶液与稀H2SO4反应:Ba2++SO42-═BaSO4↓ |
| A. | 达到化学平衡时,正反应和逆反应的速率都为零 | |
| B. | 当C、B、A的分子数比为2:1:2,反应达到平衡状态当 | |
| C. | 当单位时间消耗a mol B,同时消耗2a molA时,反应达到平衡状态 | |
| D. | B的气体的分压强不变时,反应达到平衡状态 |
| A. | 氯化钠溶液在电流作用下电离成钠离子和氯离子 | |
| B. | 溶于水能电离出氢离子的化合物都是酸 | |
| C. | 硫酸钡难溶于水,但硫酸钡属于强电解质 | |
| D. | 金属Cu能导电,但它不是电解质,是非电解质 |