题目内容
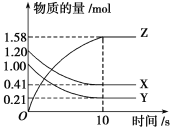
【题目】在密闭容器中发生反应:X+2Y![]() 2Z(△H<0),其中Z呈气态,且Z在平衡混合气中的体积分数(Z%)与温度(T)、压强(P)的关系如图,下列判断正确的是
2Z(△H<0),其中Z呈气态,且Z在平衡混合气中的体积分数(Z%)与温度(T)、压强(P)的关系如图,下列判断正确的是

A. Y一定呈气态
B. T1大于T2
C. 升高温度,该反应的化学平衡常数增大
D. 当c(X):c(Y):c(Z)=1:2:2时,反应达到平衡状态
【答案】A
【解析】A.根据图像可知,随着压强的增大,生成物Z的百分含量逐渐升高,说明增大压强平衡向正反应方向移动,而增大压强,平衡向气体系数和减小的方向移动,所以Y一定呈气态,故A正确;B.该反应为放热反应,若Z的百分含量增大,说明平衡正向移动,只有降低温度,平衡才正向移动,所以T1小于T2,故B错误;C.该反应为放热反应,升高温度,平衡逆向移动,该反应的化学平衡常数减小,故C错误;D.物质的物质的量浓度之比不能用来判断化学平衡状态,故D错误;故选A。

【题目】(1)下表是A、B、C、D四种有机物的有关信息:
A | ①能使溴的四氯化碳溶液退色;②比例模型为 |
B | ①由C和H两种元素组成;②比例模型为 |
C | ①由C、H、O三种元素组成;②能与Na反应,但不能与NaOH溶液反应;③能与D反应生成相对分子质量为100的酯 |
D | ①由C、H、O三种元素组成;②球棍模型为 |
回答下列问题:
①A与Br2的CCl4溶液反应的生成物的名称是________________。
②B不能使溴水因发生化学反应而褪色,B与一定比例浓硫酸和浓硝酸的混合溶液发生反应,为了使反应在50~60 ℃下进行,常用的方法是_____________;反应方程式为: ________________________________,反应类型为:________反应。
③C和D反应生成相对分子质量为100的酯,生成的酯的结构简式:______。
(2)已知: A是石油裂解气的主要成份,A的产量通常用来衡量一个国家的石油化工水平;由A通过聚合反应生成高分子化合物F,F可用于工业合成塑料,现以A为主要原料合成G, 以A为原料的合成路线如下图所示。

回答下列问题:
①D、G分子中的官能团名称分别__________、___________。
②在反应①~⑥中,属于加成反应的是________,属于取代反应的是________。(填序号)
③写出与G分子式相同的所有羧酸类的同分异构体:_______________。