题目内容
【题目】在T ℃时,铬酸银(Ag2CrO4)在水溶液中的沉淀溶解平衡曲线如图所示。下列说法中不正确的是
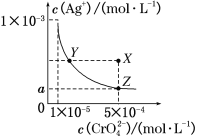
A. T ℃时,在Y点和Z点,Ag2CrO4的Ksp相等
B. 向饱和Ag2CrO4溶液中加入固体K2CrO4不能使溶液由Y点变为X点
C. 图中a=![]() ×10-4
×10-4
D. T ℃时,Ag2CrO4的Ksp为1×10-8
【答案】D
【解析】
A.一定温度下溶度积是常数,随温度变化,不随浓度变化,所以t℃时,Y点和Z点时Ag2CrO4的Ksp相等,故A正确;
B.在饱和Ag2CrO4溶液中加入K2CrO4仍为饱和溶液,点仍在曲线上,所以在饱和Ag2CrO4溶液中加入K2CrO4不能使溶液由Y点变为X点,故B正确;
C.依据溶度积常数计算Ksp(Ag2CrO4)=c2(Ag+)c(CrO42-)=1×10-11,Z点时c(CrO42-)=5×10-4,则c2(Ag+)=2×10-8,所以a=![]() ×10-4,故C正确;
×10-4,故C正确;
D.依据图象曲线上的数据结合溶度积常数概念计算得到;曲线上的点是沉淀溶解平衡,Ag2CrO4的沉淀溶解平衡为:Ag2CrO4(s)2Ag++CrO42-;Ksp=c2(Ag+)c(CrO42-)=(10-3)2×10-5=10-11;故D错误。
故选D。

练习册系列答案
相关题目