题目内容
7.常温下,下列各组离子能大量共存的是( )| A. | K+,Na+,Br-,Fe3+ | B. | H+,K+,MnO${\;}_{{4}^{\;}}$-,C2O42- | ||
| C. | K+,H+,NO3-,I- | D. | Na+,H+,SO32-,S2+ |
分析 如离子之间不发生反应生成沉淀、气体、水或不发生氧化还原反应、互促水解等反应,则可大量共存,以此解答该题.
解答 解:A.离子之间不发生任何反应,可大量共存,故A正确;
B.酸性条件下,发生氧化还原反应,MnO4-与C2O42-不能大量共存,故B错误;
C.H+,NO3-,I-发生氧化还原反应,故C错误;
D.H+,SO32-,S2+反应生成硫和水,不能大量共存,故D错误.
故选A.
点评 本题考查离子的共存,为高频考点,侧重元素化合物知识的综合理解和运用的考查,注意把握常见物质的性质,把握复分解反应、氧化还原反应的特点,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
17.不同条件下,对于工业合成氨反应:N2+3H2 ?2NH3,下列表示其反应最快的是( )
| A. | v(H2)=0.09 mol/(L•s) | B. | v(N2)=0.02 mol/(L•min) | ||
| C. | v(NH3)=0.02 mol/(L•min) | D. | v(NH3)=0.03 mol/(L•s) |
18.下列说法正确的是( )
| A. | H与D、16O与18O互为同位素,H216O、D216O、H218O、D218O互为同分异构体 | |
| B. | 金刚石、石墨均为碳的同素异形体,其化学性质与物理性质均不相同 | |
| C. | 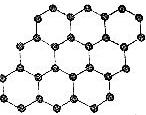 石墨烯(结构如图所示)是由碳原子构成的单层片状结构的新材料,与石墨互为同位素 | |
| D. | 由于氢原子可以形成H-(如NaH),所以有人建议可将氢元素排在元素周期表的ⅦA族 |
12.作为基本化学工业之一的氯碱工业,是通地电解饱和食盐水得到NaOH、Cl2和H2,有关电解产物的说法正确的是( )
| A. | H2不能在Cl2中燃烧 | B. | 在阳极得到H2 | ||
| C. | NaOH是弱碱 | D. | Cl2可用于制造漂白粉 |
19.保持温度不变,向NH4Cl溶液中加入一定量的水,则( )
| A. | 溶液中各离子的浓度都减小 | B. | c(Cl-)/c(NH4+)减小 | ||
| C. | c(H+)/c(NH4+)增大 | D. | c(H+)•c(OH-)减小 |
16.下列反应既属于化合反应,又属于氧化还原反应的是( )
| A. | Fe+2HCl═H2↑+FeCl2 | B. | 2FeCl2+Cl2 ═2FeCl3 | ||
| C. | CaO+H2O═Ca(OH)2 | D. | 2Fe(OH)3 $\frac{\underline{\;△\;}}{\;}$Fe2O3+3H2O |
1.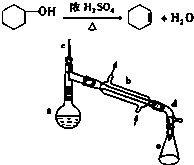 醇脱水是合成烯烃的常用方法,实验室合成己烯的反应和实验装置如图:
醇脱水是合成烯烃的常用方法,实验室合成己烯的反应和实验装置如图:
可能用到的有关数据如下:
在a中加入20g环己醇和2小片碎瓷片,冷却搅动下慢慢加入1mL浓硫酸.b中通入冷却水后,开始缓慢加热a,控制馏出物的温度不超过90℃.
分离提纯:
反应粗产物倒入分液漏斗中分别用少量5%碳酸钠溶液和水洗涤,分离后加入无水氯化钙颗粒,静置一段时间后弃去氯化钙.最终通过蒸馏得到纯净环己烯l0g.
回答下列问题:
(1)装置a的名称是蒸馏烧瓶.
(2)加入碎瓷片的作用是防止暴沸.
(3)本实验中最容易产生的副产物的结构简式为 .
.
(4)分液漏斗在使用前须检漏;在本实验分离过程中,产物应该从分液漏斗的上口倒出(填“上口倒出”或“下口放出”).
(5)分离提纯过程中加入无水氯化钙的目的是吸收水.
(6)本实验所得到的环已烯产率是C(填正确答案标号).
A.41% B.50% C.61% D.70%
 醇脱水是合成烯烃的常用方法,实验室合成己烯的反应和实验装置如图:
醇脱水是合成烯烃的常用方法,实验室合成己烯的反应和实验装置如图:可能用到的有关数据如下:
| 相对分子质量 | 密度/(g•cm-3) | 沸点/℃ | 溶解性 | |
| 环己醇 | 100 | 0.9618 | 161 | 微溶于水 |
| 环己烯 | 82 | 0.8102 | 83 | 难溶于水 |
分离提纯:
反应粗产物倒入分液漏斗中分别用少量5%碳酸钠溶液和水洗涤,分离后加入无水氯化钙颗粒,静置一段时间后弃去氯化钙.最终通过蒸馏得到纯净环己烯l0g.
回答下列问题:
(1)装置a的名称是蒸馏烧瓶.
(2)加入碎瓷片的作用是防止暴沸.
(3)本实验中最容易产生的副产物的结构简式为
 .
.(4)分液漏斗在使用前须检漏;在本实验分离过程中,产物应该从分液漏斗的上口倒出(填“上口倒出”或“下口放出”).
(5)分离提纯过程中加入无水氯化钙的目的是吸收水.
(6)本实验所得到的环已烯产率是C(填正确答案标号).
A.41% B.50% C.61% D.70%