题目内容
【题目】某校研究性学习小组用相同大小的铜片和锌片为电极研究水果电池(如图所示),得到的实验数据如下表所示:
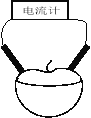
已知:西红柿、苹果果汁都是显酸性。
实验编号 | 水果种类 | 电极间距离/㎝ | 电流大小/A |
① | 西红柿 | 1 | 98.7 |
② | 西红柿 | 2 | 72.5 |
③ | 苹 果 | 2 | 27.2 |
(1)该实验的目的是探究水果种类和________对水果电池电流大小的影响。
(2)能表明水果种类对电流大小有影响的实验编号是 和 。
(3)上图所示的装置中,负极的电极反应式为 ,正极附近区域c(H+)将 (填“增大”、“减小”、“不变”),总反应离子方程式为 。
【答案】(1)电极间距离
(2)②;③
(3)Zn-2e-=Zn2+;减小;Zn+2H+=Zn2++H2↑
【解析】
试题分析:(1)①②中电极间距离不同,②③中水果种类不同,电极间距离、水果种类都导致其电流不同,所以该实验的目的是探究水果种类和电极间距对水果电池电流大小的影响。
故答案为:电极间距;
(2)②③中水果种类不同导致其电流不同,所以能表明水果种类对电流大小有影响的实验编号是②和③。
故答案为:②;③;
(3)该装置中,Zn易失电子作负极、电极反应式为:Zn-2e-=Zn2+;Cu作正极,电极反应式为:Zn+2H+=Zn2++H2↑,所以正极区c(H+)将减小。该电池总反应离子方程式为:Zn+2H+=Zn2++H2↑。
故答案为:Zn-2e-=Zn2+;减小;Zn+2H+=Zn2++H2↑。

 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案【题目】某学校化学学习小组为探究二氧化氮的性质,按下图所示装置进行实验,请回答下列问题:

(1)装置甲中盛放浓硝酸的仪器A的名称是 ,仪器B中发生反应的化学方程式为
(2)完成下面表格中的空白
装置编号 | 实验现象 | 反应的化学方程式 | NO2表现的化学性质 |
乙 | 淡黄色固体变白色 | Na2O2+2NO2=2NaNO3 | |
丙 | 氧化性 |
(3)取下装置丙中的试管C,向其中滴加足量的Na2SO3溶液,溶液颜色褪去,该过程中发生反应的离子方程式为 。
反应后的溶液中主要含有SO32—、SO42—、I—等阴离子,请填写鉴定SO32—、SO42—和I—的实验报告。
限选试剂:2mol/LHCl、1mol/LH2SO4、1mol/LBaCl2、1mol/LBa(NO3)2、CCl4、新制饱和溴水、新制饱和氯水。
编号 | 实验操作 | 预期现象和结论 |
步骤1 | 取少量待测液于试管A中,加入几滴新制得饱和溴水,振荡 | ,证明待测液中含有SO32— |
步骤2 | ||
步骤3 | 另取少量待测液于试管C中,加入足量氯水,再加入四氯化碳,振荡、静置后观察颜色 | ,证明待测液中含有I- |