题目内容
某同学设计如图所示装置分别进行探究实验(夹持装置已略去)| 实验 | 药品 | 制取气体 | 量气管中的液体 |
| ① | Cu、稀HNO3 | H2O | |
| ② | NaOH固体、浓氨水 | NH3 | |
| ③ | Na2CO3固体、稀H2SO4 | CO2 | |
| ④ | 镁铝合金、NaOH溶液(足量) | H2 | H2O |
(1)简述如何检查该装置的气密性: .
(2)该同学认为实验①可通过收集测量NO气体的体积,来探究Cu样品的纯度.你认为是否可行?请简述原因. .
(3)实验②、③中,量气管中的液体最好分别是 、 .(只选一种)
A.H2OB.CCl4C.饱和Na2CO3溶液 D.饱和NaHCO3溶液
(4)本实验应对量气管多次读数,读数时应注意:
①恢复至室温,② ,③视线与凹液面最低处相平.
(5)实验④获得以下数据(所有气体体积均已换算成标准状况)根据上述合理数据计算镁铝合金中铝的质量分数 .
| 编号 | 镁铝合金质量 | 量气管第一次读数 | 量气管第二次读数 |
| 1 | 1.0g | 10.0mL | 347.5mL |
| 2 | 1.0g | 10.0mL | 335.0mL |
| 3 | 1.0g | 10.0mL | 344.5mL |

【答案】分析:(1)设法使装置内外形成气压差,是气密性检查的常用手段;
(2)根据一氧化氮气体的性质判断,一氧化氮和氧气能发生生成易和水反应的二氧化氮气体,据此分析.
(3)量气管中液体的选择标准是:和该气体不反应.
(4)对量气管读数时,首先等实验装置恢复到室温再进行下一步操作,然后调节量气管使左右液面相平,最后读数时视线与凹液面最低处相平.
(5)实验④,铝和氢氧化钠反应,根据量气管的第二次读数-第一次读数=生成氢气的体积,求出生成氢气的平均值,再求出合金中铝的质量,最后计算出镁铝合金中铝的质量分数.
解答:解:(1)关闭开关A和分液漏斗活塞,微热烧瓶,量气管左端液面升高,说明气密性良好
(2)一氧化氮与氧气反应生成二氧化氮,二氧化氮可与水反应生成一氧化氮和硝酸;装置中有空气,一氧化氮会与装置中的空气反应,生成的二氧化氮溶于水并与水反应,使测得的一氧化氮体积不准,所以不可以通过实验收集并测量NO气体的体积来探究铜样品的纯度;
故答案为:不可行.因为NO会与装置中空气反应后溶于水,使测得的NO气体体积不准.
(3)实验②中氨气极易溶于水,所以量气管中液体不能选用水及水溶液,只能选和氨气不反应的四氯化碳;实验③中的气体是二氧化碳,二氧化碳能溶于水,四氯化碳有毒,碳酸钠和二氧化碳能反应,二氧化碳和饱和的碳酸氢钠不反应,所以选取饱和碳酸氢钠溶液.
故答案为:B、D.
(4)根据PV=nRT,为保证测出来的气体体积是当时大气压下的体积,在读数时应注意:①将实验装置恢复到室温,②使量气管两端液面相平,因为相平说明两边液面上的压强是一样的,这样测出来的气体体积才是当时大气压下的体积,③视线与凹液面最低处相平,俯视或仰视会造成误差;
故答案为:使量气管两端液面相平.
(5)铝和氢氧化钠反应生成氢气的体积=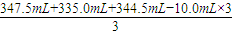 =332.3mL=0.3323L,
=332.3mL=0.3323L,
设生成0.997L氢气,需铝的质量为x
2Al+2NaOH+2H2O═2NaAlO2+3H2↑
54g 67.2L
x 0.3323L
x=0.27g
所以铝的质量分数为 =27%
=27%
故答案为:27%.
点评:本题考查了测定气体体积的方法,难度不大,易错题是量气管中液体的选择,选择标准是和该气体不反应.
(2)根据一氧化氮气体的性质判断,一氧化氮和氧气能发生生成易和水反应的二氧化氮气体,据此分析.
(3)量气管中液体的选择标准是:和该气体不反应.
(4)对量气管读数时,首先等实验装置恢复到室温再进行下一步操作,然后调节量气管使左右液面相平,最后读数时视线与凹液面最低处相平.
(5)实验④,铝和氢氧化钠反应,根据量气管的第二次读数-第一次读数=生成氢气的体积,求出生成氢气的平均值,再求出合金中铝的质量,最后计算出镁铝合金中铝的质量分数.
解答:解:(1)关闭开关A和分液漏斗活塞,微热烧瓶,量气管左端液面升高,说明气密性良好
(2)一氧化氮与氧气反应生成二氧化氮,二氧化氮可与水反应生成一氧化氮和硝酸;装置中有空气,一氧化氮会与装置中的空气反应,生成的二氧化氮溶于水并与水反应,使测得的一氧化氮体积不准,所以不可以通过实验收集并测量NO气体的体积来探究铜样品的纯度;
故答案为:不可行.因为NO会与装置中空气反应后溶于水,使测得的NO气体体积不准.
(3)实验②中氨气极易溶于水,所以量气管中液体不能选用水及水溶液,只能选和氨气不反应的四氯化碳;实验③中的气体是二氧化碳,二氧化碳能溶于水,四氯化碳有毒,碳酸钠和二氧化碳能反应,二氧化碳和饱和的碳酸氢钠不反应,所以选取饱和碳酸氢钠溶液.
故答案为:B、D.
(4)根据PV=nRT,为保证测出来的气体体积是当时大气压下的体积,在读数时应注意:①将实验装置恢复到室温,②使量气管两端液面相平,因为相平说明两边液面上的压强是一样的,这样测出来的气体体积才是当时大气压下的体积,③视线与凹液面最低处相平,俯视或仰视会造成误差;
故答案为:使量气管两端液面相平.
(5)铝和氢氧化钠反应生成氢气的体积=
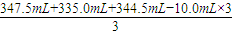 =332.3mL=0.3323L,
=332.3mL=0.3323L,设生成0.997L氢气,需铝的质量为x
2Al+2NaOH+2H2O═2NaAlO2+3H2↑
54g 67.2L
x 0.3323L
x=0.27g
所以铝的质量分数为
 =27%
=27%故答案为:27%.
点评:本题考查了测定气体体积的方法,难度不大,易错题是量气管中液体的选择,选择标准是和该气体不反应.

练习册系列答案
相关题目
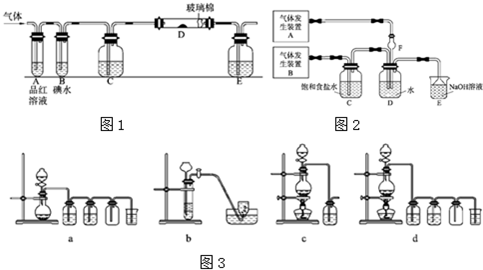
如图1所示是实验室中制取气体的一种简易装置.

(1)请简述检验它的气密性的方法 .
(2)利用如图1所示装置可以制取(填反应物状况及发生反应是否需要的条件) 气体.
(3)某同学设计如图2所示装置,用粗铁粒与16.9%稀硝酸反应制取NO气体并探究产物中铁的价态.请回答有关问题.已知16.9%稀硝酸的密度为1.10g/cm3,则其物质的量浓度为 (计算结果保留两位小数).用若用63%的硝酸配制16.9%稀硝酸500mL,所需的玻璃仪器有玻璃棒、烧杯和 .
(4)当打开止水夹a、关闭止水夹b时,A装置的干燥管中观察到的现象是 .B装置烧杯中液体的作用是 .当A装置中气体几乎无色时,打开止水夹b,关闭止水夹a,可用C装置收集NO气体.
(5)已知下列反应可以发生:Fe2O3+3KNO3+4KOH
2K2FeO4+3KNO2+2H2O,而A装置中的稀硝酸即使换成浓硝酸,也不能生成+6价的铁的化合物,其原因是 .
a.HNO3的氧化性比KNO3弱
b.反应的温度不够
c.HNO3的热稳定性比KNO3差
d.FeO42-不能存在于酸性溶液中
(6)现有仪器和药品:试管和胶头滴管,0.1mol/L KSCN溶液、0.2mol/L酸性KMnO4溶液、0.1mol/L KI溶液、氯水等.请你设计一个简单实验,探究A装置烧杯里完全反应后含铁可能的价态,填写表中实验报告:

(1)请简述检验它的气密性的方法
(2)利用如图1所示装置可以制取(填反应物状况及发生反应是否需要的条件)
(3)某同学设计如图2所示装置,用粗铁粒与16.9%稀硝酸反应制取NO气体并探究产物中铁的价态.请回答有关问题.已知16.9%稀硝酸的密度为1.10g/cm3,则其物质的量浓度为
(4)当打开止水夹a、关闭止水夹b时,A装置的干燥管中观察到的现象是
(5)已知下列反应可以发生:Fe2O3+3KNO3+4KOH
| 高温 |
a.HNO3的氧化性比KNO3弱
b.反应的温度不够
c.HNO3的热稳定性比KNO3差
d.FeO42-不能存在于酸性溶液中
(6)现有仪器和药品:试管和胶头滴管,0.1mol/L KSCN溶液、0.2mol/L酸性KMnO4溶液、0.1mol/L KI溶液、氯水等.请你设计一个简单实验,探究A装置烧杯里完全反应后含铁可能的价态,填写表中实验报告:
| 实验步骤 | 操作 | 现象与结论 |
| 第一步 | 取少量液体装于试管,向试 管中滴入几滴KSCN溶液. |
|
| 第二步 | 若溶液紫色褪去,则说明含有Fe2+; 若无明显变化,则说明不含Fe2+. |