题目内容
(15分)铁、铝、铜等金属及其化合物在日常生活中应用广泛,请根据下列实验回答问题:
(1)单质铁属于______晶体,将FeCl3溶液加热蒸干,灼烧所得的物质是______ (填化学式):
(2)请写出铝与氢氧化钠溶液反应的化学方程式______________________________
(3)金属Cu单独与氨水或单独与双氧水都不反应,但可与二者的混合溶液反应生成深蓝色溶液,在该深蓝色的浓溶液中加入乙醇所产生的现象是______,画出呈深蓝色的离子的结构式______.
写出Cu与氨水、双氧水反应的离子方程式:____________________________________.
(4)在硫酸亚铁溶液中加入过量的碳酸氢铵,有FeCO3沉淀生成,写出其化学方程式____________.
(1)单质铁属于______晶体,将FeCl3溶液加热蒸干,灼烧所得的物质是______ (填化学式):
(2)请写出铝与氢氧化钠溶液反应的化学方程式______________________________
(3)金属Cu单独与氨水或单独与双氧水都不反应,但可与二者的混合溶液反应生成深蓝色溶液,在该深蓝色的浓溶液中加入乙醇所产生的现象是______,画出呈深蓝色的离子的结构式______.
写出Cu与氨水、双氧水反应的离子方程式:____________________________________.
(4)在硫酸亚铁溶液中加入过量的碳酸氢铵,有FeCO3沉淀生成,写出其化学方程式____________.
(1)金属晶体(1分),Fe2O3(2分)
(2)2Al+2NaOH+2H2O=2NaAlO2+3H2↑(3分)
(3)析出深蓝色晶体(1分)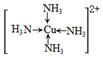 (2分)
(2分)
Cu+4NH3·H2O+H2O2=[Cu(NH3)4]2++4H2O+2OH-(3分)
(4)FeSO4+2NH4HCO3=FeCO3↓+CO2↑+(NH4)2SO4+H2O(3分)
(2)2Al+2NaOH+2H2O=2NaAlO2+3H2↑(3分)
(3)析出深蓝色晶体(1分)
 (2分)
(2分)Cu+4NH3·H2O+H2O2=[Cu(NH3)4]2++4H2O+2OH-(3分)
(4)FeSO4+2NH4HCO3=FeCO3↓+CO2↑+(NH4)2SO4+H2O(3分)
试题分析:(1)单质铁属于金属晶体,FeCl3溶液存在Fe3+ + 3H2O
 Fe(OH)3 + 3H+,加热蒸干促进水解生成氢氧化铁沉淀、灼烧氢氧化铁分解得Fe2O3;(2)铝与氢氧化钠溶液反应生成偏铝酸钠和氢气,化学方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑;(3)金属Cu与双氧水发生氧化还原反应,生成的铜离子随即与一水合氨中的氮形成配位键,这种离子化合在乙醇中溶解度小而析出深蓝色晶体,其结构为
Fe(OH)3 + 3H+,加热蒸干促进水解生成氢氧化铁沉淀、灼烧氢氧化铁分解得Fe2O3;(2)铝与氢氧化钠溶液反应生成偏铝酸钠和氢气,化学方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑;(3)金属Cu与双氧水发生氧化还原反应,生成的铜离子随即与一水合氨中的氮形成配位键,这种离子化合在乙醇中溶解度小而析出深蓝色晶体,其结构为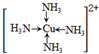 ,离子方程式是Cu+4NH3?H2O+H2O2=[Cu(NH3)4]2++4H2O+2OH-;(4)在硫酸亚铁溶液中加入过量的碳酸氢铵,有FeCO3沉淀生成,同时碳酸氢根离子电离出的氢离子与碳酸氢根离子结合成二氧化碳和水,化学方程式为FeSO4+2NH4HCO3=FeCO3↓+CO2↑+(NH4)2SO4+H2O。
,离子方程式是Cu+4NH3?H2O+H2O2=[Cu(NH3)4]2++4H2O+2OH-;(4)在硫酸亚铁溶液中加入过量的碳酸氢铵,有FeCO3沉淀生成,同时碳酸氢根离子电离出的氢离子与碳酸氢根离子结合成二氧化碳和水,化学方程式为FeSO4+2NH4HCO3=FeCO3↓+CO2↑+(NH4)2SO4+H2O。
练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目