题目内容
【题目】亚硝酰氯(NOCl)是一种红褐色液体或黄色气体,沸点为-5.5℃,遇水和潮气分解。
回答下列问题:
(1)NO与Cl2在通常条件下可反应得到NOCl。某实验小组用浓盐酸与MnO2反应制C12,Cu和稀HNO3制NO。
①制取NO的离子方程式为________________________
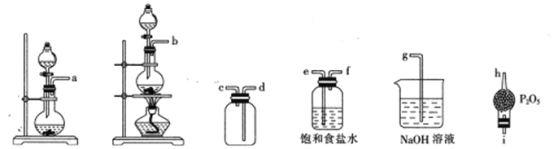
②选用下列部分装置预制备一瓶干燥纯净的氯气,各玻璃导管接口连接顺序为____(气流方向从左至右)。
(2)文献中记录的一种利用浓盐酸和NaNO2浓溶液反应制取NOCl的原理及装置如下所示:
反应原理:NaNO2+2HCl=NOCl↑+NaCl+H2O。制取装置图:
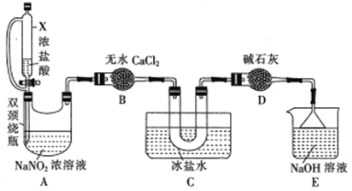
①仪器X的名称为_______,用它代替分液漏斗的优点是_________________
②装置C的U形管中观察到的现象是____________,装置D的作用是_________
(3)取少量产品NOCl滴入盛有水的试管中,液面上方有白雾且产生无色气体,该气体在试管口变为红棕色,NOCl与水反应的化学方程式为___________________
【答案】3Cu+8H++2NO3―=3Cu2++2NO↑+4H2O b→e→f→i→h→d→c→g 恒压分液漏斗 便于浓盐酸顺利滴入三颈烧瓶中 有红褐色液体生成 防止水蒸气进入U形管中,同时除去尾气中NOCl等酸性气体 3NOCl+2H2O=HNO3+3HCl+2NO↑
【解析】
(1)①Cu和稀HNO3反应生成硝酸铜、一氧化氮和水;
②浓盐酸与MnO2共热反应制得的C12中混有挥发出的氯化氢气体,应用饱和食盐水除去氯气,用酸性干燥剂干燥氯气,用向上排空气法收集氯气,并用氢氧化钠溶液吸收尾气中的氯气,防止污染空气;
(2)①仪器X的名称为恒压分液漏斗,与分液漏斗相比,恒压分液漏斗能起到平衡气压的作用,便于浓盐酸顺利滴入三颈烧瓶中;
②由题意可知,亚硝酰氯沸点为-5.5℃,温度低于-5.5℃时会冷凝变为红褐色液体;注意亚硝酰氯遇水和潮气分解,冷凝收集时要注意防止水蒸气进入U形管中;
(3)由题意可知,亚硝酰氯液体与水反应生成硝酸、盐酸和一氧化氮气体;
(1)①Cu和稀HNO3反应生成硝酸铜、一氧化氮和水,反应的离子方程式为3Cu+8H++2NO3―=3Cu2++2NO↑+4H2O,故答案为:3Cu+8H++2NO3―=3Cu2++2NO↑+4H2O;
②浓盐酸与MnO2共热反应制得C12,制得的C12中混有挥发出的氯化氢气体,将气体通过盛有饱和食盐水的洗气瓶除去极易溶于水的氯化氢气体,再将气体通过盛有五氧化二磷的干燥管,干燥氯气,因氯气密度比空气大,应用向上排空气法收集氯气,因氯气有毒,应用氢氧化钠溶液吸收氯气,防止污染空气,则制备一瓶干燥纯净的氯气,各玻璃导管接口连接顺序为b→e→f→i→h→d→c→g,故答案为:b→e→f→i→h→d→c→g;
(2)①仪器X的名称为恒压分液漏斗,与分液漏斗相比,恒压分液漏斗能起到平衡气压的作用,便于浓盐酸顺利滴入三颈烧瓶中,故答案为:恒压分液漏斗;便于浓盐酸顺利滴入三颈烧瓶中;
②由题意可知,亚硝酰氯沸点为-5.5℃,装置C中冰盐水的作用是冷凝亚硝酰氯,则U形管中可收集到红褐色亚硝酰氯液体;因亚硝酰氯遇水和潮气分解,则装置D中碱石灰的作用是防止水蒸气进入U形管中,导致亚硝酰氯遇水和潮气分解,同时吸收尾气中NOCl等酸性气体,故答案为:有红褐色液体生成;防止水蒸气进入U形管中,同时除去尾气中NOCl等酸性气体;
(3)由题意可知,亚硝酰氯液体与水反应生成硝酸、盐酸和一氧化氮气体,反应的化学方程式为3NOCl+2H2O=HNO3+3HCl+2NO↑,故答案为:3NOCl+2H2O=HNO3+3HCl+2NO↑。