题目内容
A、B、C、D、E是五种中学常见的单质,已知A、B、C、D在常温下均为气体。E是地壳中含量居第二位的金属。D可分别跟A、B、C在一定的条件下化合,生成X、Y、Z;Y、Z与Ne的电子数相等,A是第三周期的元素。有关的转化关系如下图所示(反应条件均已略去):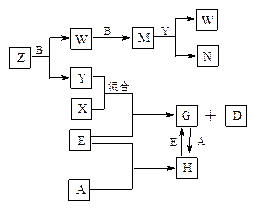
(1)A的化学式为 ,B的化学式为 ,C的电子式为 。
(2)Z和W在催化剂和加热的条件下反应生成C和Y,这是一个很有意义的反应,可以消除W对环境的污染,该反应的化学方程式为 。
(3)将N溶液滴入G的溶液中会产生W,写出上述变化的离子反应方程式:
。
(4)Z与N恰好反应后产物溶解在水中,所得溶液的pH(填“大于”、“小于”或“等于”) 7,用离子反应方程式表示其原因为 。
(14分)(1)Cl2(2分) O2(2分) 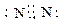 (2分)
(2分)
(2)6NO+4NH3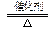 5N2+6H2O(2分)(3)4H++NO3–+3Fe2+
5N2+6H2O(2分)(3)4H++NO3–+3Fe2+ NO↑+2H2O+3Fe3+(2分)
NO↑+2H2O+3Fe3+(2分)
(4)小于7(2分) NH4++H2O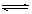 NH3·H2O+H+(2分)
NH3·H2O+H+(2分)
解析

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
已知A、B、C、D、E是短周期原子序数依次增大的五种元素,A原子在元素周期表中原子半径最小,B与E同主族,且E的原子序数是B的两倍,C、D是金属,它们的氢氧化物均难溶于水.下列说法不正确的是( )
| A、简单离子的半径:C>D>E>B | B、工业上常用电解法制得C和D的单质 | C、稳定性:A2B>A2E | D、单质D可用于冶炼某些难熔金属 |

 2DB3,若3.2gDB2完全转化为DB3气体时放热akJ;1mol DB3气体完全转化为其水化物放热bkJ,则标况下33.6L DB2完全完成上述两步反应放热
2DB3,若3.2gDB2完全转化为DB3气体时放热akJ;1mol DB3气体完全转化为其水化物放热bkJ,则标况下33.6L DB2完全完成上述两步反应放热
