题目内容
【题目】用 NA 表示阿伏加德罗常数的值,下列说法中正确的是( )
①1mol Na2O 和 Na2O2 混合物中含有的阴、阳离子总数是 3NA
②常温常压下,92g的NO2和N2O4 混合气体含有的原子数为 6NA
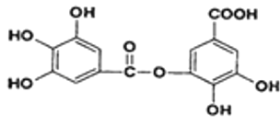
③7.8 g![]() 中含有的碳碳双键数目为 0.3 NA
中含有的碳碳双键数目为 0.3 NA
④用 1L1.0 mol/LFeCl3 溶液制备氢氧化铁胶体,所得氢氧化铁胶粒的数目为 NA
⑤1mol SO2与足量O2在一定条件下充分反应生成 SO3,共转移 2NA个电子
⑥在反应 KIO3+6HI=KI+3I2+3H2O 中,每生成 3molI2 转移的电子数为 5NA
A.①②③B.②③④C.①②⑥D.④⑤⑥
【答案】C
【解析】
①Na2O和Na2O2中阴、阳离子个数之比都为1:2,1mol Na2O和Na2O2混合物中含有的阴、阳离子总物质的量为3mol,阴、阳离子总数是 3NA,故①正确;
②NO2和N2O4的实验式都是NO2,n(NO2)=![]() =2mol,常温常压下92g的NO2和N2O4混合气体中所含原子物质的量为6mol,含有的原子数为 6NA,故②正确;
=2mol,常温常压下92g的NO2和N2O4混合气体中所含原子物质的量为6mol,含有的原子数为 6NA,故②正确;
③苯中不含碳碳双键,故③错误;
④n(FeCl3)=1.0mol/L×1L=1mol,根据反应FeCl3+3H2O![]() Fe(OH)3(胶体)+3HCl,生成1molFe(OH)3,氢氧化铁胶粒是一定数目Fe(OH)3的集合体,氢氧化铁胶粒的物质的量小于1mol,氢氧化铁胶粒的数目小于 NA,故④错误;
Fe(OH)3(胶体)+3HCl,生成1molFe(OH)3,氢氧化铁胶粒是一定数目Fe(OH)3的集合体,氢氧化铁胶粒的物质的量小于1mol,氢氧化铁胶粒的数目小于 NA,故④错误;
⑤若1molSO2全部反应则转移2mol电子,而SO2与O2的反应是可逆反应,1molSO2与足量O2在一定条件下充分反应生成SO3,转移电子物质的量小于2mol,转移电子数小于2NA,故⑤错误;
⑥用双线桥分析该反应: ,每生成3molI2转移5mol电子,转移的电子数为 5NA,故⑥正确;
,每生成3molI2转移5mol电子,转移的电子数为 5NA,故⑥正确;
①②⑥正确,故答案选C。

【题目】下列我国科研成果所涉及材料中,主要成分为同主族元素形成的无机非金属材料的是
|
|
|
|
A.4.03米大口径碳化硅反射镜 | B.2022年冬奥会聚氨酯速滑服 | C.能屏蔽电磁波的碳包覆银纳米线 | D.“玉兔二号”钛合金筛网轮 |
A. AB. BC. CD. D