题目内容
【题目】图为实验室某盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:

(1)该浓盐酸中HCl的物质的量浓度为______mol·L-1。
(2)取用任意体积的该盐酸溶液时,下列物理量中不随所取体积的多少而变化的是______;
A.溶液中HCl的物质的量 B.溶液的浓度
C.溶液中Cl-的数目 D.溶液的密度
(3)某学生欲用上述浓盐酸和蒸馏水配制480mL物质的量浓度为 0.400mol·L-1的稀盐酸。
①容量瓶上需标有以下五项中的________。
A.温度 B.浓度 C.容量 D.压强 E.刻度线
②将下列操作填写完整,并排列其正确的操作顺序________(用字母表示,每个字母只能用一次);
A.用少量蒸馏水洗涤________2~3次,并将洗涤液全部转移到容量瓶中,再加适量蒸馏水,振荡容量瓶,使溶液混合均匀。
B.用量筒准确量取浓盐酸 ________mL,注入烧杯中,加入少量水(约30mL),用玻璃棒慢慢搅拌,使其混合均匀。
C.将已冷却的盐酸沿玻璃杯注入________中。
D.盖好瓶塞,颠倒摇匀,装瓶,贴签。
E.改用__________加水,至_____________________________。
F.继续往容量瓶内小心加水,直到液面接近刻度________处。
③在配制过程中,下列实验操作对所配制的稀盐酸物质的量浓度有何影响? (在横线上天“偏大”、“偏小”、“无影响”)
a.用量筒量取浓盐酸时俯视观察凹液面__________;
b.洗涤量取浓盐酸后的量筒,并将洗涤液转移到容量瓶中__________;
c.定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水___________;
d.定容时仰视刻度线__________。
【答案】 11.9 BD ACE BCAFED 烧杯和玻璃棒 16.8 500ml 容量瓶 胶头滴管 液体凹液面与刻度线相切 1--2cm 偏小 偏大 偏小 偏小
【解析】试题分析:(1)根据c=![]() 计算 HCl的物质的量浓度。
计算 HCl的物质的量浓度。
(2)溶液是均一、稳定的混合物,所以取用任意体积的该盐酸溶液时,A、根据n=cV分析正误;B、根据溶液是均一、稳定的混合物分析正误;C、n=cV分析溶液中Cl-的数目;D、根据溶液是均一、稳定的混合物分析正误。
(3)①①根据容量瓶上标示判断;②根据稀释过程中溶质的质量不变列式计算需要该浓盐酸的体积。根据配制一定物质的量浓度溶液的步骤分析;
③根据cB=nB/V可得,一定物质的量浓度溶液配制的误差都是由溶质的物质的量nB和溶液的体积V引起的。误差分析时,关键要看配制过程中引起n和V怎样的变化。在配制一定物质的量浓度溶液时,若nB比理论值小,或V比理论值大时,都会使所配溶液浓度偏小;若nB比理论值大,或V比理论值小时,都会使所配溶液浓度偏大。
解析:根据以上分析,(1)根据c=![]() 可知,该浓盐酸中HCl的物质的量浓度c=
可知,该浓盐酸中HCl的物质的量浓度c=![]() mol/L=11.9mol/L。
mol/L=11.9mol/L。
(2)溶液是均一、稳定的混合物,所以取用任意体积的该盐酸溶液时,A、根据n=cV可知,溶液中HCl的物质的量与溶液的体积、浓度有关系,故A错误;B、溶液的浓度是不变的,总是11.9mol/L,故B正确;C、溶液中Cl-的数目与溶液的体积、浓度有关系,故C错误;D、溶液的密度是溶液的性质,与溶液的体积无关系,故D正确。
(3)①①容量瓶上标示有A.温度;C.容量;E.刻度线。
②配制浓度为0.4mol![]() L-1体积为480mL的稀盐酸,实验室没有480mL容量瓶,所以选用500mL容量瓶,需要配制500mL溶液;根据稀释过程中溶质的质量不变可知,配制500 mL物质的量浓度为0.400 mol·L-1的稀盐酸需要该浓盐酸的体积=
L-1体积为480mL的稀盐酸,实验室没有480mL容量瓶,所以选用500mL容量瓶,需要配制500mL溶液;根据稀释过程中溶质的质量不变可知,配制500 mL物质的量浓度为0.400 mol·L-1的稀盐酸需要该浓盐酸的体积=![]() =0.0168L=16.8mL。
=0.0168L=16.8mL。
配制500mL浓度为0.4mol![]() L-1的稀盐酸的步骤为:计算、量取、稀释、冷却、转移、洗涤、定容、摇匀等,所以正确的操作顺序是:B.用量筒准确量取浓盐酸16.8mL,注入烧杯中,加入少量水(约30mL),用玻璃棒慢慢搅拌,使其混合均匀。C.将已冷却的盐酸沿玻璃杯注入:500mL容量瓶中;A.用少量蒸馏水洗涤烧杯、玻璃棒2~3次,并将洗涤液全部转移到容量瓶中,再加适量蒸馏水,振荡容量瓶,使溶液混合均匀。F.继续往容量瓶内小心加水,直到液面接近刻度液体1--2cm处;E.改用胶头滴管加水,至液体凹液面与刻度线相切;D.盖好瓶塞,颠倒摇匀,装瓶,贴签。
L-1的稀盐酸的步骤为:计算、量取、稀释、冷却、转移、洗涤、定容、摇匀等,所以正确的操作顺序是:B.用量筒准确量取浓盐酸16.8mL,注入烧杯中,加入少量水(约30mL),用玻璃棒慢慢搅拌,使其混合均匀。C.将已冷却的盐酸沿玻璃杯注入:500mL容量瓶中;A.用少量蒸馏水洗涤烧杯、玻璃棒2~3次,并将洗涤液全部转移到容量瓶中,再加适量蒸馏水,振荡容量瓶,使溶液混合均匀。F.继续往容量瓶内小心加水,直到液面接近刻度液体1--2cm处;E.改用胶头滴管加水,至液体凹液面与刻度线相切;D.盖好瓶塞,颠倒摇匀,装瓶,贴签。
③根据cB=nB/V,在配制一定物质的量浓度溶液时,若nB比理论值小,或V比理论值大时,都会使所配溶液浓度偏小;若nB比理论值大,或V比理论值小时,都会使所配溶液浓度偏大。a.用量筒量取浓盐酸时俯视观察凹液面,浓盐酸物质的量减小,所配稀溶液的浓度偏小;
b.洗涤量取浓盐酸后的量筒,并将洗涤液转移到容量瓶中,浓盐酸物质的量增大,所以所配稀溶液的浓度偏大;
c.定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水,溶液体积偏大,所配稀溶液的浓度偏小;
d.定容时仰视刻度线,溶液体积偏大,所配稀溶液的浓度偏小。

 阅读快车系列答案
阅读快车系列答案【题目】Ⅰ.如图所示,一密闭容器被无摩擦、可滑动的两隔板a、b分成甲、乙两室;标准状况下,在乙室中充入NH30.4mol,甲室中充入HCl、N2的混合气体,静止时隔板位置如图所示。已知甲、乙两室中气体的质量之差为17.3g。
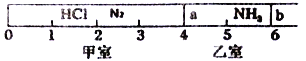
(1)甲室中HCl、N2的质量之比为__________________。
(2)将隔板a去掉,一段时间后,隔板b将稳定位于刻度“________’’处(填数字,不考虑固体物质产生的压强),此时体系的平均相对分子质量为________。
Ⅱ.已知硫酸、氨水的密度与所加水的量的关系如图所示,现有硫酸与氨水各一份,请根据表中信息,回答下列问题:
溶质的物质的量浓度/molL-1 | 溶液的密度/gcm-3 | |
硫酸 | c1 | ρ1 |
氨水 | c2 | ρ2 |
(1)表中硫酸的质量分数为________(不写单位,用含c1、ρ1,的代数式表示)。
(2)物质的量浓度为c1molL-1的硫酸与水等体积混合(混合后溶液的体积变化忽略不计),所得溶液的物质的量浓度为________molL-1。
(3)将物质的量浓度分别为c2molL-1和0.2c2molL-1的氨水等质量混合,所得溶液的物质的量浓度__________0.6c2molL-1(填“大于”、“小于”或“等于”)(设混合后溶液的体积变化忽略不计)
Ⅲ.电解法处理含氮氧化物废气,可回收硝酸,具有较高的环境效益和经济效益。实验室模拟电解法吸收NOx的装置如图所示(图中电极均为石墨电极)。

若用NO2气体进行模拟电解法吸收实验。
①写出电解时NO2发生反应的电极反应式:_________________________________。
②若有标准状况下2.24LNO2被吸收,通过阳离子交换膜的H+为________mol。