题目内容
19.下列说法正确的是( )| A. | 铅笔芯的原材料为铅,儿童使用铅笔时如果用嘴吮咬能够引起铅中毒 | |
| B. | 酸雨形成的主要原因是汽车尾气的任意排放 | |
| C. | 维生素C受热更易被氧化,故有些新鲜蔬菜生吃较好 | |
| D. | 淀粉、纤维素,、蛋白质和油脂均属于天然高分子化合物 |
分析 A.从铅笔芯的原材料分析,应为石墨而不是铅;
B.酸雨形成的主要原因是燃烧含硫的燃料如煤会生成二氧化硫;
C.根据温度越高,维生素C损失越多;
D.根据高分子化合物是指相对分子质量很大的有机物,可达几万至几十万,甚至达几百万或更大.
解答 解:A.铅笔芯的原材料为石墨,虽然无毒,但儿童也不能随便用嘴吮咬,防止扎伤,故A错误;
B.酸雨形成的主要原因是燃烧含硫的燃料如煤会生成二氧化硫,故B错误;
C.根据温度越高,维生素C损失越多,因此生吃新鲜蔬菜比熟吃蔬菜维生素C的损失小,故C正确;
D.淀粉、纤维素、蛋白质的相对分子质量在一万以上,属于有机高分子化合物,油脂相对分子质量较小,不属于高分子化合物,故D错误;
故选C.
点评 本题主要考查了物质的分类、性质等知识,题目难度不大,注意基础知识的积累.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
9.阿司匹林是人们熟知的感冒药,是第一个重要的人工合成药物,具有解热镇痛作用.其化学名为乙酰水杨酸,可由水杨酸与乙酸酐直接反应制得,二者的结构简式为: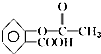 (阿司匹林)、
(阿司匹林)、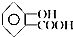 (水杨酸).下列有关二者所含官能团的说法正确的是( )
(水杨酸).下列有关二者所含官能团的说法正确的是( )
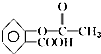 (阿司匹林)、
(阿司匹林)、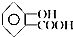 (水杨酸).下列有关二者所含官能团的说法正确的是( )
(水杨酸).下列有关二者所含官能团的说法正确的是( )| A. | 均含有碳碳双键 | B. | 均含酯基和羟基 | C. | 均为芳香化合物 | D. | 均含羧基和苯基 |
10.在恒容密闭容器中,可逆反应H2(g)+I2(g)?2HI(g)达到平衡时的标志是( )
| A. | 1个I-I键断裂的同时,有2个H-I键断裂 | |
| B. | H2、I2、HI的浓度相等 | |
| C. | 混合气体的质量不再改变 | |
| D. | 混合气体密度恒定不变 |
7.等物质的量的PCl5(g)分别放入起始体积相同的恒压容器A和恒容容器B中,相同温度下反应:PCl5(g)?PCl3(g)+Cl2(g)达到平衡时,两容器中PCl5的分解率相比(用X表示)( )
| A. | XA>XB | B. | XA<XB | C. | XA=XB | D. | 无法确定 |
14.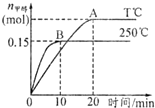 将1mol CO和2mol H2充入一容积为1L的密闭容器中,分别在250°C、T°C下发生反应:CO(g)+2H2(g)?CH3OH(g).
将1mol CO和2mol H2充入一容积为1L的密闭容器中,分别在250°C、T°C下发生反应:CO(g)+2H2(g)?CH3OH(g).
根据右图,下列分析中正确的是( )
 将1mol CO和2mol H2充入一容积为1L的密闭容器中,分别在250°C、T°C下发生反应:CO(g)+2H2(g)?CH3OH(g).
将1mol CO和2mol H2充入一容积为1L的密闭容器中,分别在250°C、T°C下发生反应:CO(g)+2H2(g)?CH3OH(g).根据右图,下列分析中正确的是( )
| A. | 250°C时,反应在前10 s 的平均速率v(H2)=0.015 mol/(L.min) | |
| B. | 平衡时CO的转化率:250°C>T0C | |
| C. | 反应达平衡后,其他条件不变,若减小容积体积,CO体积分数增大 | |
| D. | 该反应的正反应是放热反应 |
4.下列各组元素中,已知A、B两种元素的原子序数,其中可组成AB3型离子化合物的是( )
| A. | 6和9 | B. | 13和9 | C. | 11和8 | D. | 12和17 |
11.下列叙述正确的是( )
| A. | 48 g O3气体含有6.02×1023个O3分子 | |
| B. | 常温常压下,4.6g NO2气体含有1.81×1023个NO2分子 | |
| C. | 0.5mol/LCuCl2溶液中含有3.01×1023个Cu2+ | |
| D. | 标准状况下,33.6L 水含有9.03×1023个H2O分子 |
8.下列实验方案不能达到实验目的是( )
| 实验目的 | 实验方案 | |
| A | 证明溴乙烷发生消去反应有乙烯生成 | 向试管中加入适量的溴乙烷和NaOH的乙醇溶液,加热,将反应产生的气体通入溴的四氯化碳溶液 |
| B | 确定苯中是否有酒精 | 向苯和酒精的混合液中加入金属钠 |
| C | 检验蔗糖水解产物具有还原性 | 向蔗糖溶液中加入几滴稀硫酸,水浴加热几分钟,然后加入适量稀NaOH溶液,再向其中加入新制的银氨溶液,并水浴加热 |
| D | 检验制得气体是否为乙烯 | C2H5OH与浓硫酸170℃共热,制得的气体通入酸性KMnO4溶液 |
| A. | A | B. | B | C. | C | D. | D |