题目内容
10.在酸性溶液中,能大量共存的离子是( )| A. | Mg2+、Fe2+、NO3-、ClO- | B. | Al3+、Mg2+、Cl-、SO42- | ||
| C. | K+、Na+、Cl-、HSO3- | D. | Na+、K+、NO3-、SiO32- |
分析 A.硝酸根离子在酸性条件下能够氧化亚铁离子,次氯酸离子能够氧化亚铁离子,还能够与氢离子结合生成次氯酸;
B.四种离子之间不发生反应,都不与酸性溶液中的氢离子反应;
C.亚硫酸氢根离子与酸性溶液中的氢离子反应生成二氧化硫气体;
D.硅酸根离子与氢离子结合生成硅酸沉淀.
解答 解:A.Fe2+、NO3-之间在酸性溶液中能够发生氧化还原反应,ClO-能够氧化Fe2+,ClO-能够与结合生成次氯酸,在溶液中不能大量共存,故A错误;
B.Al3+、Mg2+、Cl-、SO42-之间不反应,都不与酸性溶液中的氢离子反应,在溶液中能够大量共存,故B正确;
C.HSO3-与酸性溶液中的氢离子反应,在溶液中不能大量共存,故C错误;
D.SiO32-与酸性溶液中的氢离子反应生成硅酸,在溶液中不能大量共存,故D错误;
故选B.
点评 本题考查离子共存的判断,为中等难度的试题,注意明确离子不能大量共存的一般情况,如:能发生复分解反应的离子之间,能发生氧化还原反应的离子之间等;解决离子共存问题时还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-.

练习册系列答案
 学习实践园地系列答案
学习实践园地系列答案
相关题目
5.生活中我们常用到铝制餐具.铝在空气中稳定存在的原因是( )
| A. | 铝能产生铝热反应 | B. | 铝的化学性质不活泼 | ||
| C. | 常温下铝不能与氧气反应 | D. | 铝表面能形成致密的氧化膜 |
15.下列关于碱金属元素和卤素的说法中,错误的是( )
| A. | 钾与水的反应比钠与水的反应更剧烈 | |
| B. | 溴单质与水的反应比氯单质与水的反应更剧烈 | |
| C. | 随核电荷数的增加,碱金属元素和卤素的原子半径都逐渐增大 | |
| D. | 碱金属元素中,锂原子失去最外层电子的能力最弱 |
2.用NA表示阿伏德罗常数,下列叙述正确的是( )
| A. | 物质的量浓度为0.5mol•L-1的MgCl2溶液中,含有Cl-个数为1 NA | |
| B. | 标准状况下,11.2 L S03含有的分子数为0.5NA | |
| C. | 1 mol Na2O2含离子数为4NA | |
| D. | 24 g O2分子和24 g O3分子所含的氧原子数目相等 |
19.欲迅速除去铁壶底的水垢,最好的办法是用( )
| A. | 浓盐酸 | B. | 稀硝酸 | C. | 浓硫酸 | D. | 浓硝酸 |

 或
或 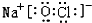 .
.
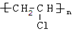 .
.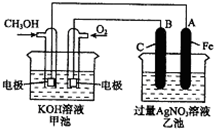 如图是一个化学过程的示意图.
如图是一个化学过程的示意图.