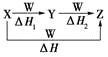题目内容
【题目】已知可逆反应X(g)+2Y(g)![]() Z(g) ΔH <0,一定温度下,在体积为2 L的密闭容器中加入4 mol Y和一定量的X后,X的浓度随时间的变化情况如图所示,则下列说法正确的是( )
Z(g) ΔH <0,一定温度下,在体积为2 L的密闭容器中加入4 mol Y和一定量的X后,X的浓度随时间的变化情况如图所示,则下列说法正确的是( )

A. 若向该容器中加入1molX、2molY,达平衡时,X的平衡浓度小于0.125mol/L
B. a点正反应速率大于逆反应速率
C. 反应达平衡时,降低温度可以实现c到d的转化
D. 该条件下,反应达平衡时,平衡常数K=3
【答案】B
【解析】
试题A.根据图像可知,在反应开始时加入2molX 、4molY,二者的物质的量的比是1:2,若向该容器中加入1molX、2molY,二者的物质的量的比也是1:2,该反应是反应前后气体体积相等的反应,所以改变压强,化学平衡不发生移动,则当达到平衡时X的浓度是原来的1/2,c(X)=0.125mol/L,错误;B.根据题意可知反应从正反应方向开始,到c点时达到化学化学平衡,此时正反应速率与逆反应速率相等,所以在达到平衡前的a点,正反应速率大于逆反应速率,正确;C.反应达平衡时,降低温度化学平衡向放热的正反应方向移动,反应物的浓度会降低,所以不可能实现c到d的转化,错误;D.该条件下,反应达平衡时,平衡常数,各种物质的浓度分别是c(X)=0.25mol/L,c(Y)=0.5mol/L,c(Z)=0.75mol/L,所以该反应的化学平衡常数K= c(Z)÷[c(X)×c2(Y)]= 0.75÷[0.25×0.52]=12,错误。

练习册系列答案
 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案
相关题目