题目内容
1.按要求写出方程式.(1)写出NaHCO3在水溶液里的电离方程式NaHCO3═Na++HCO3-.
(2)硫酸铜与氢氧化钡反应(写出离子方程式)Cu2++SO42-+Ba2++2OH-═Cu(OH)2↓+BaSO4↓.
(3)NaHSO4+NaOH═Na2SO4+H2O(写出离子方程式)H++OH-═H2O.
分析 (1)为强电解质,完全电离生成钠离子、碳酸氢根离子;
(2)反应生成硫酸钡和氢氧化铜;
(3)反应实质为氢离子与氢氧根离子生成水.
解答 解:(1)为强电解质,完全电离生成钠离子、碳酸氢根离子,电离方程式为NaHCO3═Na++HCO3-,故答案为:NaHCO3═Na++HCO3-;
(2)反应生成硫酸钡沉淀和氢氧化铜沉淀,离子方程式为Cu2++SO42-+Ba2++2 OH-═Cu(OH)2↓+BaSO4↓,
故答案为:Cu2++SO42-+Ba2++2OH-═Cu(OH)2↓+BaSO4↓;
(3)NaHSO4+NaOH═Na2SO4+H2O的反应实质为氢离子与氢氧根离子生成水,离子反应为H++OH-═H2O,故答案为:H++OH-═H2O.
点评 本题考查离子反应方程式及电离方程式,为高频考点,把握电解质的强弱及离子反应的书写方法为解答的关键,侧重分析与应用能力的考查,综合性较强,题目难度不大.

练习册系列答案
 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案
相关题目
12.下列说法不正确的是( )
| A. | 需要持续加热才能发生的反应一定是吸热反应 | |
| B. | MnO2能加速H2O2的分解,是因为MnO2可以降低反应所需的活化能 | |
| C. | 分别稀释10mLpH=1的盐酸和醋酸至100mL,后者pH变化大,说明醋酸是弱酸 | |
| D. | 向橙色的K2Cr2O7溶液中滴加NaOH溶液,溶液颜色变黄,说明化学平衡发生了移动 |
9.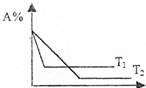 可逆反应A(g)+2B(g)?C(g) 在相同压强时,混和气体中A的百分含量跟反应时间t、温度T的关系如图所示,下列结论正确是( )
可逆反应A(g)+2B(g)?C(g) 在相同压强时,混和气体中A的百分含量跟反应时间t、温度T的关系如图所示,下列结论正确是( )
 可逆反应A(g)+2B(g)?C(g) 在相同压强时,混和气体中A的百分含量跟反应时间t、温度T的关系如图所示,下列结论正确是( )
可逆反应A(g)+2B(g)?C(g) 在相同压强时,混和气体中A的百分含量跟反应时间t、温度T的关系如图所示,下列结论正确是( )| A. | T1>T2,正反应是放热反应 | B. | T1>T2,正反应是吸热反应 | ||
| C. | T2>T1,正反应是放热反应 | D. | T2>T1,正反应是吸热反应 |
10.把V L含有MgS04和K2S04的混合溶液分成5等份,一份加入含a mol NaOH的溶液,恰好使镁离子完全沉淀为氢氧化镁;另一份加入含b mol BaCl2的溶液,恰好使硫酸根离子完全沉淀为硫酸钡.则原混合溶液中钾离子的浓度为( )
| A. | $\frac{b-2a}{V}$ | B. | $\frac{2b-5a}{V}$ | C. | $\frac{10b-5a}{V}$ | D. | $\frac{5a-10b}{V}$ |
 .
.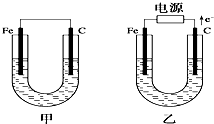 如图所示,甲、乙两池电极材料都是铁棒和碳棒,请回答下列问题:
如图所示,甲、乙两池电极材料都是铁棒和碳棒,请回答下列问题: