题目内容
(16分)硫酸是一种实验室常用的化学试剂。请按要求填空:
(1)浓硫酸试剂瓶上适合贴上的图标是 (填写字母标号)。
(2)实验室有1.00mol·L-1的硫酸溶液,从中准确量出10.00 mL,其物质的量浓度为 mol·L-1。现将准确量出的10.00 mL的硫酸溶液配制成0.100mol·L-1的稀硫酸,所需要的玻璃仪器除烧杯、玻璃棒还需 和 。
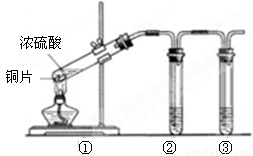
(3)用图所示的实验装置验证铜与浓硫酸反应生成的气体产物,则装置②、③分别为 。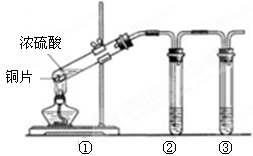
A.品红溶液 B.BaCl2溶液 C.NaOH溶液 D.AgNO3溶液
(4)装置①中发生反应的化学方程式为 ,
若装置①中加入铜6.4g和含有0.2molH2SO4的浓硫酸,则产生二氧化硫质量
A.等于6.4克 B.大于6.4克 C.小于6.4克 D.不能确定
(5)若将装置①中的铜片换成木炭,装置②试管内为品红溶液, 装置③试管内为澄清石灰水,则装置①中发生反应的化学方程式为 。装置②中的现象是 。根据装置③观察到有白色沉淀生成的现象 , (填“能”或“不能”)判断该白色沉淀一定只有CaCO3。
(共16分)
(1)C(1分) (2) 1.00(1分);胶头滴管(1分);100mL容量瓶(1分) (3)A(1分);C(1分)
(3)A(1分);C(1分) (4)Cu+2H2SO4(浓)="==" CuSO4+SO2↑+2H2O (2分) C(2分)
(4)Cu+2H2SO4(浓)="==" CuSO4+SO2↑+2H2O (2分) C(2分)
(5)C+2H2SO4(浓)=== CO2+2SO2↑+2H2O(2分)
溶液由红色变为无色(2分) 不能(2分)
解析试题分析:(1)浓硫酸具有强氧化性,有很强的腐蚀性。(2)在同一个溶液中的浓度是相等的。配置溶液需要的仪器有,烧杯、玻璃棒、胶头滴管、100mL容量瓶。(3)②中验证SO2用的是品红溶液。③中是进行尾气吸收用的是NaOH溶液。(4)①中发生的是铜和浓硫酸的反应,方程式为:Cu+2H2SO4(浓)="==" CuSO4+SO2↑+2H2O,因为浓硫酸反应过程中浓度越来越稀,到最后呈稀硫酸就不和铜反应了,故产生二氧化硫质量小于6.4克。(5)①中发生的是炭和浓硫酸的反应,方程式为:C+2H2SO4(浓)=== CO2+2SO2↑+2H2O,SO2通入到中品红溶液褪色,因为SO2能和反应生成沉淀,所以不能判断该白色沉淀一定只有CaCO3。
考点:化学实验
点评:本题重点考查的是浓硫酸的氧化性的相关知识,题中涉及到的化学反应均为课本中的,学生要注重对课本知识的学习。