题目内容
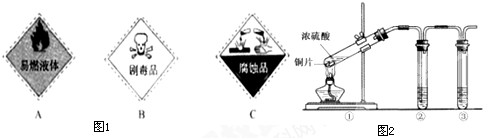
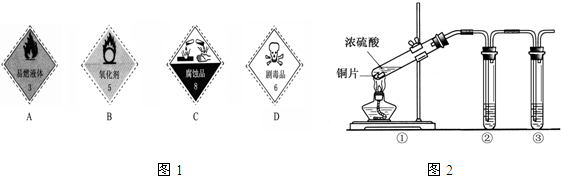
硫酸是一种实验室常用的化学试剂,请按要求填空:(1)浓硫酸试剂瓶上适合贴上的图标是(图1)
(2)实验室用1.0mol?L-1的硫酸配制0.10mol?L-1的稀硫酸100mL,所需要的玻璃仪器为烧杯、玻璃棒、胶头滴管、酸式滴定管和
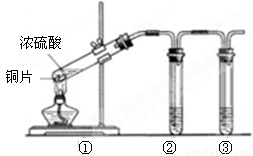
(3)用图2所示的实验装置②验证铜与浓硫酸反应的还原产物,则装置②、③中试剂依次为
分析:(1)根据浓硫酸具有腐蚀性、强氧化性进行分析;
(2)配制溶液时用到的玻璃仪器有烧杯、量筒、玻璃棒、胶头滴管以及容量瓶等仪器;
(3)铜和浓硫酸反应生成二氧化硫,结合二氧化硫的性质检验及完成处理方法进行解答.
(2)配制溶液时用到的玻璃仪器有烧杯、量筒、玻璃棒、胶头滴管以及容量瓶等仪器;
(3)铜和浓硫酸反应生成二氧化硫,结合二氧化硫的性质检验及完成处理方法进行解答.
解答:解:(1)浓硫酸具有腐蚀性,适合贴上的图标是图中的C;浓硫酸具有强氧化性,应该贴上B氧化剂,
故答案为:BC;
(2)根据配制一定物质的量浓度的溶液步骤可知,配制溶液时用到的玻璃仪器有:烧杯、量筒、玻璃棒、胶头滴管以及100mL容量瓶等仪器,还缺少100 mL容量瓶,
故答案为:100mL容量瓶;
(3)铜和浓硫酸反应生成二氧化硫,二氧化硫具有漂白性,可选用品红检验,因二氧化硫有毒,不能排放到空气中,可用氢氧化钠吸收,
故答案为:品红溶液(或溴水,或酸性高锰酸钾溶液等);氢氧化钠溶液.
故答案为:BC;
(2)根据配制一定物质的量浓度的溶液步骤可知,配制溶液时用到的玻璃仪器有:烧杯、量筒、玻璃棒、胶头滴管以及100mL容量瓶等仪器,还缺少100 mL容量瓶,
故答案为:100mL容量瓶;
(3)铜和浓硫酸反应生成二氧化硫,二氧化硫具有漂白性,可选用品红检验,因二氧化硫有毒,不能排放到空气中,可用氢氧化钠吸收,
故答案为:品红溶液(或溴水,或酸性高锰酸钾溶液等);氢氧化钠溶液.
点评:本题综合考查浓硫酸的性质,侧重于学生的分析能力、实验能力的考查,为高考常见题型和高频考点,注意把握浓硫酸的性质,难度不大.

练习册系列答案
相关题目