题目内容
【题目】下列装置或操作能达到目的的是( )
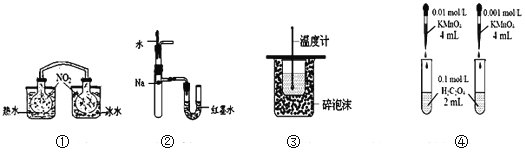
A. 装置①依据两容器内气体颜色变化,不能判断反应2NO2(g)![]() N2O4(g)平衡移动的方向
N2O4(g)平衡移动的方向
B. 装置②依据U管两边液面的高低判断Na和水反应的热效应
C. 装置③测定中和热
D. 装置④依据褪色快慢比较浓度对反应速率的影响
【答案】B
【解析】
A. NO2是红棕色气体,2NO2(g)![]() N2O4(g)颜色加深表明平衡逆向移动,装置①依据两容器内气体颜色变化,能判断反应2NO2(g)
N2O4(g)颜色加深表明平衡逆向移动,装置①依据两容器内气体颜色变化,能判断反应2NO2(g)![]() N2O4(g)平衡移动的方向,故不选A;
N2O4(g)平衡移动的方向,故不选A;
B. 钠与水反应放热,温度升高,大试管内温度升高,气体膨胀,U型管左侧液面降低,装置②可以依据U管两边液面的高低判断Na和水反应的热效应,故选B;
C. 装置③中没有环形玻璃搅拌器,不能测定中和热,故不选C;
D. 两种高锰酸钾的浓度不同,颜色不同,不符合控制变量法,应保证高锰酸钾浓度相同,用不同浓度的草酸来做实验,故不选D;
本题答案选B。

 习题精选系列答案
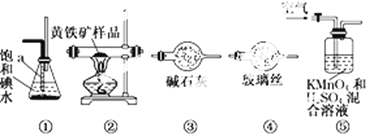
习题精选系列答案【题目】工业上可用下列仪器组装一套装置来测定黄铁矿(主要成分FeS2)中硫的质量分数(忽略SO2、H2SO3与氧气的反应)。实验的正确操作步骤如下:
A.连接好装置,并检查装置的气密性
B.称取研细的黄铁矿样品
C.将2.0 g样品小心地放入硬质玻璃管中
D.以1 L/min的速率鼓入空气
E.将硬质玻璃管中的黄铁矿样品加热到800℃~850℃
F.用300 mL的饱和碘水吸收SO2,发生的反应是:I2+SO2+2H2O = 2HI+H2SO4
G.吸收液用CCl4萃取、分离
H.取20.00mLG中所得溶液,用0.2000mol·L-1的NaOH标准溶液滴定。试回答:
(1)步骤G中所用主要仪器是______,应取_______ (填“上”或“下”)层溶液进行后续实验。
(2)装置正确的连接顺序是 ![]()
![]()
![]() ④
④ ![]() (填编号)。______
(填编号)。______
(3)装置⑤中高锰酸钾的作用是__________。持续鼓入空气的作用__________。
(4)步骤H中滴定时应选用_____作指示剂,可以根据________现象来判断滴定已经达到终点。
(5)假定黄铁矿中的硫在操作E中已全部转化为SO2,并且被饱和碘水完全吸收,滴定得到的数据如下表所示:
滴定次数 | 待测液的体积/mL | NaOH标准溶液的体积/mL | |
滴定前 | 滴定后 | ||
第一次 | 20.00 | 0.00 | 20.48 |
第二次 | 20.00 | 0.22 | 20.20 |
第三次 | 20.00 | 0.36 | 20.38 |
则黄铁矿样品中硫元素的质量分数为___________。
(6)也有人提出用“沉淀质量法”测定黄铁矿中含硫质量分数,若用这种方法测定,最好是在装置①所得吸收液中加入下列哪种试剂__________ 。
A.硝酸银溶液 B.氯化钡溶液 C.澄清石灰水 D.酸性高锰酸钾溶液