题目内容
【题目】NA代表阿伏加德罗常数的值,下列叙述正确的是
A. 标准状况下,1.12 L CCl4含有质子数的数目为3.7NA
B. 常温常压下,3.0 g含葡萄糖的冰醋酸中含有的原子总数为0.4NA
C. 常温时,56g Fe与足量浓硝酸反应,转移的电子数目为3NA
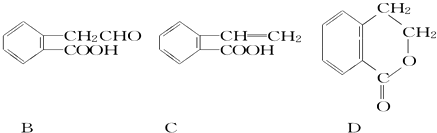
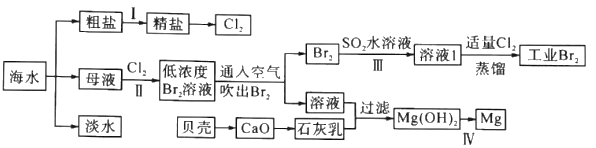
D. 晶体B的结构单元如右图 ,则11g晶体B含有0.6NA个三角形(相邻原子构成)
,则11g晶体B含有0.6NA个三角形(相邻原子构成)
【答案】B
【解析】A、标况下,CCl4是液体,故A错误;B、葡萄糖(C6H12O6)的冰醋酸(C2H4O2)的混合物,最简式为(CH2O)n,3.0 g混合物中有0.1mol CH2O,故原子总数为0.4NA,故B正确;C、常温时,56g Fe与足量浓硝酸钝化,故C错误;D、B的晶体中,一个三角形有三个B,每个B参与形成5个三角形,故一个三角形有0.6个B,则11gB,即为1molB含有的三角形数为5/3NA,故D错误;故选B。

 名校课堂系列答案
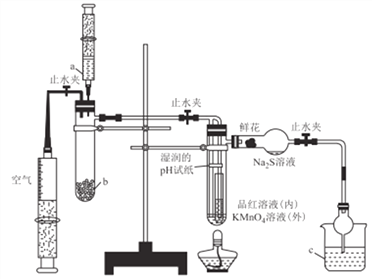
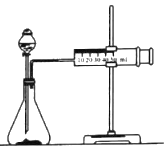
名校课堂系列答案【题目】化学反应速率是描述化学反应进行快慢程度的物理量。某学生为了探究镁条与盐酸反应过程中反应速率的变化,利用如图装置测定一定时间内反应放出氢气的体积(加入稀盐酸的体积为100mL.忽略反应中溶液体积的变化),实验记录如下表(累计值):
时间(min) | l | 2 | 3 | 4 | 5 | 6 |
氢气体积(mL)(标准状况) | 1 | 50 | 120 | 232 | 288 | 310 |
(1)除如图所示的实验用品外,还需要的一件实验仪器是_________。
(2)实验前,检查该装置气密性的方法是_________。
(3)装置气密性良好,0~lmin时间段氢气体积却很少的原因是_________。
(4)反应速率最大的时间段是_________min(填“0~1”1~2”2~3”3~4”“4~5”或“5~6”),原因是_________(从影响反应速率因素的角度解释)。
(5)3~4min时间段,以盐酸的浓度变化来表示的该反应速率为_________(设溶液体积不变)。
(6)由于反应太快,测量氢气体积时不好控制,他就事先在盐酸溶液中分别加入等体积的下列液体以减慢反应速率,你认为不可行的是_________(填相应字母)。
A.蒸馏水 B.KCl溶液 C.KNO3溶液 D.CuSO4溶液