题目内容
(7分)化学键的键能是指气态原子间形成1mol化学键时释放的能量。如:H(g)+I(g)→H-I(g)+297KJ 即H-I键的键能为297kJ/mol,也可以理解为破坏1mol H-I键需要吸收297KJ的热量。化学反应的发生可以看成旧化学键的破坏和新化学键的形成。下表是一些键能数据。(单位:kJ/mol)
阅读上述信息,回答下列问题:
(1)根据表中数据判断CCl4的稳定性 (填“大于”或“小于”)CF4的稳定性。试预测C-Br键的键能范围_________< C-Br键能 <__________
(2)有人认为:H-O键的键能大于H-S键的键能,所以H2O的熔沸点高于H2S的熔沸点。你是否赞同这种观点?如不赞同,请说出你的解释。
(3)已知H2O(l)=H2O(g) ΔH=+44kJ/mol,请写出表示氢气燃烧热的热化学方程式:
| | 键能 | | 键能 | | 键能 |
| H-H | 436 | Cl-Cl | 243 | H-Cl | 432 |
| S=S | 255 | H-S | 339 | C-F | 427 |
| C-Cl | 330 | C-I | 218 | H-F | 565 |
| C-O | 347 | H-O | 464 | Si—Si | 176 |
| Si—O | 460 | O=O | 497 | | |
阅读上述信息,回答下列问题:
(1)根据表中数据判断CCl4的稳定性 (填“大于”或“小于”)CF4的稳定性。试预测C-Br键的键能范围_________< C-Br键能 <__________
(2)有人认为:H-O键的键能大于H-S键的键能,所以H2O的熔沸点高于H2S的熔沸点。你是否赞同这种观点?如不赞同,请说出你的解释。
(3)已知H2O(l)=H2O(g) ΔH=+44kJ/mol,请写出表示氢气燃烧热的热化学方程式:
(1)小于 218~330 KJ·mol-1
(2) 不赞同,H2O的熔沸点高于H2S是因为水分子间存在氢键,与键能无关。
(3) H2(g)+1/2O2(g)=H2O(l) △H="-287.5" kJ/mo1
(2) 不赞同,H2O的熔沸点高于H2S是因为水分子间存在氢键,与键能无关。
(3) H2(g)+1/2O2(g)=H2O(l) △H="-287.5" kJ/mo1
(1)共价键的键能越大,分子越稳定,所以四氯化碳的稳定性小于四氟化碳的。溴的非金属性介于氯和碘之间,所以C-Br键的键能大于C-I的键能,小于C-Cl的键能。
(2)键能大小影响分子的稳定性,和熔沸点大小无关。水的熔沸点高于硫化氢的是因为水中存在氢键。
(3)在一定条件下,1mol可燃物完全燃烧生成稳定的氧化物时所放出的热量叫燃烧热。根据有关键能可计算出生成1mol气态水时反应热为436 kJ/mol+0.5×497 kJ/mol-2×464 kJ/mol=-243.5 kJ/mol。又因为1mol气态水变成液态水时放出44 kJ的能量,所以氢气的燃烧热是-243.5 kJ/mol-44 kJ/mol=-87.5 kJ/mo1。
(2)键能大小影响分子的稳定性,和熔沸点大小无关。水的熔沸点高于硫化氢的是因为水中存在氢键。
(3)在一定条件下,1mol可燃物完全燃烧生成稳定的氧化物时所放出的热量叫燃烧热。根据有关键能可计算出生成1mol气态水时反应热为436 kJ/mol+0.5×497 kJ/mol-2×464 kJ/mol=-243.5 kJ/mol。又因为1mol气态水变成液态水时放出44 kJ的能量,所以氢气的燃烧热是-243.5 kJ/mol-44 kJ/mol=-87.5 kJ/mo1。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
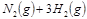
 2NH3(g))在工业生产中的大量运用,满足了人口的急剧增长对粮食的需求,也为化工生产提供了足够的原料。按要求回答下列问题:
2NH3(g))在工业生产中的大量运用,满足了人口的急剧增长对粮食的需求,也为化工生产提供了足够的原料。按要求回答下列问题: