题目内容
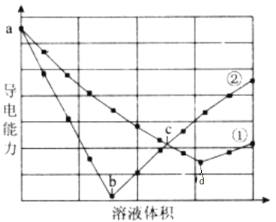
【题目】一定温度下,固定容积的密闭容器中发生下列反应:![]() 反应过程中,各物质浓度与时间的关系如图:
反应过程中,各物质浓度与时间的关系如图:

(1)该反应平衡常数表达式为![]() ____________。
____________。
(2)![]() 化学反应速率表示
化学反应速率表示![]() ______;建立平衡过程中,混合气体的密度______(选填“增大”、“减小”或“不变”)。
______;建立平衡过程中,混合气体的密度______(选填“增大”、“减小”或“不变”)。
(3)![]() 时改变外界条件,使
时改变外界条件,使![]() ______
______![]() (选填“大于”、“小于”或“等于”)。
(选填“大于”、“小于”或“等于”)。
【答案】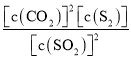
![]() 增大 大于
增大 大于
【解析】
(1)反应平衡常数表达式为各生成物浓度的化学计量数次幂的乘积除以各反应物浓度的化学计量数次幂的乘积所得的比值,固体浓度为1,故该反应平衡常数表达式为![]()
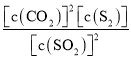 ;
;
(2)![]() 内△c(SO2)=(1.0-0.4)mol/L=0.6mol/L,故
内△c(SO2)=(1.0-0.4)mol/L=0.6mol/L,故![]() 化学反应速率表示
化学反应速率表示![]() mol/(L·min);该反应从开始到第一次平衡时,因C(s)转化为气体,故气体的总质量在不断增大,反应过程中容器体积恒定,根据
mol/(L·min);该反应从开始到第一次平衡时,因C(s)转化为气体,故气体的总质量在不断增大,反应过程中容器体积恒定,根据![]() 可知,建立平衡过程中,混合气体的密度逐渐增大;
可知,建立平衡过程中,混合气体的密度逐渐增大;
(3)30min时改变条件,由图知30min后CO2浓度下降,S2浓度上升,判断改变的条件应该是减小CO2浓度,平衡正向移动,因此![]() 。
。

练习册系列答案
相关题目
【题目】在一定温度下,10 mL 0.40 mol/L H2O2溶液发生催化分解,不同时刻测得生成O2的体积(已折算为标准状况)如下表。忽略溶液体积变化,下列叙述不正确的是
t/min | 0 | 2 | 4 | 6 | 8 | 10 |
V(O2)/mL | 0.0 | 9.6 | 16.8 | 22.4 | 26.5 | 29.9 |
A.该反应可用MnO2、FeCl3溶液作为催化剂
B.0~4 min的平均反应速率v(H2O2)=3.75×10-2mol/(L·min)
C.0~10 min,过氧化氢的分解速率逐渐加快
D.反应到6 min时,H2O2分解了50%