题目内容
17.将2份等物质的量的铁粉分别与足量的稀硫酸和稀盐酸反应,则下列说法正确的是( )| A. | 最终所得两种溶液的质量不相等 | |
| B. | 标准状况下,两者产生的氢气的体积相等 | |
| C. | 两个实验中,铁粉均有剩余 | |
| D. | 比较两个实验中铁粉失去的电子数目,前者多,后者少 |
分析 A.两种酸的质量不知道,不能确定反应后溶液的质量关系;
B.等质量的铁与足量的酸反应生成的氢气相同;
C.酸足量,Fe完全反应;
D.等质量的铁,转移的电子相同.
解答 解:A.2份等物质的量的铁粉分别与足量的稀硫酸和稀盐酸反应,两种酸的质量不知道,不能确定反应后溶液的质量关系,故A错误;
B.等质量的铁与足量的酸反应,Fe完全反应,酸有剩余,所以生成的氢气相同,标准状况下,两者产生的氢气的体积相等,故B正确;
C.2份等物质的量的铁粉分别与足量的稀硫酸和稀盐酸反应,酸足量,Fe完全反应,铁粉没有剩余,故C错误;
D.等质量的铁完全反应,转移的电子的物质的量相同,即中铁粉失去的电子数目相同,故D错误.
故选B.
点评 本题考查了Fe与酸的反应,题目难度不大,侧重于基础知识的考查,注意把握题意:酸过量,铁完全反应.

练习册系列答案
相关题目
7.关于如图所示的原电池装置,下列说法不正确的是( )
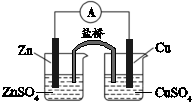

| A. | 锌是负极,发生氧化反应 | B. | 盐桥中的K+移向ZnSO4溶液 | ||
| C. | 锌电极失e-通过电流计流向铜电极 | D. | 铜电极上的反应为Cu2++2e-═Cu |
8.下列有关铁及其化合物的说法中不正确的是( )
| A. | 工业上在高温下可用CO还原含Fe2O3的铁矿石炼铁 | |
| B. | 铁在纯氧中燃烧或高温下与水蒸气反应均能得到Fe3O4 | |
| C. | 先滴加氯水,再滴加KSCN溶液后显红色证明溶液含有Fe2+ | |
| D. | 氯化铁溶液有较强氧化性,氯化铁也可用作净水剂 |
20.下列各组物质中,分子数相同的是( )
| A. | 2L SO2和2L CO2 | B. | 9g水和标准状况下11.2L CO2 | ||
| C. | 标准状况下1mol氧气和22.4L水 | D. | 0.2mol H2S和2.24L HCl |
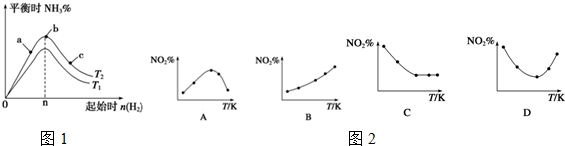
1.氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用,减少氮的氧化物在大气中的排放是环境保护的重要内容之一.
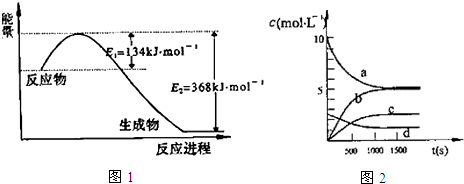
(1)如图1是1mol NO2气体和1mol CO气体反应生成CO2气体和NO气体过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:NO2(g)+CO(g)═CO2(g)+NO(g)△H=-234kJ•mol-1;
已知:N2(g)+2NO2(g)?4NO(g)△H=+292.3kJ•mol-1,
则反应:2NO(g)+2CO(g)?N2(g)+2CO2(g)的△H=-760.3kJ•mol-1;
(2)一定温度下,在体积为2L的恒容密闭容器中充入20mol NO2和5mol O2发生反应:4NO2(g)+O2(g)?2N2O5(g);已知体系中n(NO2)随时间变化如表:
①写出该反应的平衡常数表达式:K=$\frac{{c}^{2}({N}_{2}{O}_{5})}{{c}^{4}(N{O}_{2})×c({O}_{2})}$,
已知:K3000C>K3500C,则该反应是放热反应(填“放热”或“吸热”);
②反应达到平衡后,NO2的转化率为49.6%,若要增大NO2的转化率,可采取的措施有AD
A.降低温度 B.充入氦气,使体系压强增大 C.再充入NO2 D.再充入4mol NO2和1mol O2
③图2中表示N2O5的浓度的变化曲线是c,用O2表示从0~500s内该反应的平均速率v=0.00151 mol•L-1•s-1.
(1)如图1是1mol NO2气体和1mol CO气体反应生成CO2气体和NO气体过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:NO2(g)+CO(g)═CO2(g)+NO(g)△H=-234kJ•mol-1;

已知:N2(g)+2NO2(g)?4NO(g)△H=+292.3kJ•mol-1,
则反应:2NO(g)+2CO(g)?N2(g)+2CO2(g)的△H=-760.3kJ•mol-1;
(2)一定温度下,在体积为2L的恒容密闭容器中充入20mol NO2和5mol O2发生反应:4NO2(g)+O2(g)?2N2O5(g);已知体系中n(NO2)随时间变化如表:
| t(s) | 0 | 500 | 1000 | 1500 |
| n(NO2)(mol) | 20 | 13.96 | 10.08 | 10.08 |
已知:K3000C>K3500C,则该反应是放热反应(填“放热”或“吸热”);
②反应达到平衡后,NO2的转化率为49.6%,若要增大NO2的转化率,可采取的措施有AD
A.降低温度 B.充入氦气,使体系压强增大 C.再充入NO2 D.再充入4mol NO2和1mol O2
③图2中表示N2O5的浓度的变化曲线是c,用O2表示从0~500s内该反应的平均速率v=0.00151 mol•L-1•s-1.
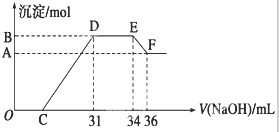
 室温下,用0.10mol•L-1KOH溶液滴定10.00mL 0.10mol•L-1H2C2O4(二元弱酸)溶液所得的滴定曲线如图(混合溶液的体积可看成混合前两溶液的体积之和).请回答下列问题:
室温下,用0.10mol•L-1KOH溶液滴定10.00mL 0.10mol•L-1H2C2O4(二元弱酸)溶液所得的滴定曲线如图(混合溶液的体积可看成混合前两溶液的体积之和).请回答下列问题: