题目内容
NA为阿伏加德罗常数的值,下列有关叙述不正确的是
A.0.1 mol C3H6Cl2中化学键总数为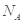 |
B.42 g乙烯中含碳原子数为3 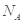 |
C.标准状况下,1L苯完全燃烧生成的气态产物的分子数为(6/22. 4)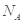 |
D.0.1 mol乙醇完全燃烧所消耗的氧分子数一定为0.3 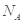 |
C
解析试题分析:标准状况下苯为液体,不能根据气体摩尔体积求出物质的量,故C错误;一个C3H6Cl2分子中含两个碳氯键、6个碳氢键、2个碳碳键,共10条化学键,故0.1molC3H6Cl2中化学键总数为NA,A正确;乙烯的最简式为CH2,42g中含CH23mol,含碳原子数为3NA;D、根据乙醇燃烧的化学方程式或耗氧量的计算方法可得D正确;故选C。
考点:有机物中化学键的判断、一定质量的烯烃中碳原子数的计算、气体摩尔体积的运用、有机物耗氧量的计算

练习册系列答案
相关题目
若用NA表示阿伏加德罗常数的值,下列叙述不正确的是
| A.1 mol BrCl与H2O完全反应生成氯化氢和次溴酸,转移的电子数为NA |
| B.锌与一定浓度的浓硫酸反应,产生标准状况下SO2和H2的混合气体22.4 L,锌失去电子数为2NA |
| C.常温常压下,20 g D2O含有的原子总数为3NA |
| D.标准状况下,44.8 L NO与22.4 L O2混合后气体中分子总数小于2NA |
设NA为阿伏加德罗常数的数值,下列说法中正确的是
| A.1mol Fe2+与足量的H2O2溶液反应,转移2nA个电子 |
| B.标准状况下,22.4L NO2气体中含有NA个O2分子 |
| C.常温常压下,15g HCHO含有2NA对共用电子对 |
| D.1L 0.1mol?L-1的醋酸溶液中有NA个CH3COO- |
用NA表示阿伏加德罗常数。下列说法正确的是
| A.12 g NaHSO4固体中含有的离子数为0.3 NA |
| B.足量Cl2与5.6 g Fe完全反应时,转移的电子数为0.2 NA |
| C.标准状况下,0.56 L 丙烷中含有的共价键数为0.25 NA |
| D.电解精炼铜时每转移NA个电子,阳极溶解32 g铜 |
NA为阿伏加德罗常数,下列说法正确的是( )
| A.106gNa2CO3晶体中的离子总数大于3NA |
| B.0.2mol Zn与一定量浓H2SO4恰好完全反应,生成的气体分子数为0.2NA |
| C.将2mL 0.5mol·L-lNa2SiO3溶液滴入稀盐酸中制得H4SiO4胶体,所含胶粒数为0.001NA |
| D.电解精炼铜时,当阳极上质量减少6.4g时,电路上转移的电子数目为0.2NA |
NA为阿伏加德罗常数,下列叙述正确的是
| A.14 gC2H4和C3H6的混合气体中含有的原子数为3NA |
| B.25 ℃时,1 L pH=13的氢氧化钡溶液中含有0.2NA个氢氧根离子 |
| C.5.6克铁与一定量稀硝酸完全反应,电子转移数目一定为0.3NA |
| D.1.0L1mol/L的NaOH水溶液中含有的氧原子数目为2 NA |
设NA为阿伏加德罗常数的值。下列叙述正确的是
| A.标准状况下,2.24LCl2溶于水,转移的电子数目为0.1NA |
| B.常温下,10 L pH=12的Na2CO3溶液中含有的OH-离子数为0.1NA |
| C.标准状况下,22.4 LNO2和NO的混合气体中所含的氮原子总数为2NA |
| D.将含有1molFeCl3的浓溶液完全水解可得到Fe(OH)3胶粒的数目为 NA |
下列实验或生产过程中发生的变化是物理变化的是( )
①在鸡蛋白溶液中加入(NH4)2SO4后形成沉淀;②用渗析的方法除去混在Fe(OH)3胶体中的FeCl3;③NO2经加压凝聚成无色的液体;④溴水滴入植物油中振荡褪色;⑤水泥、沙子和水混合后硬化;⑥照相底片感光
| A.①②③ | B.②④⑥ |
| C.①② | D.③⑤ |
用NA表示阿伏加德罗常数的值。下列叙述中正确的是
| A.78 g 苯含有碳碳双键的数目为3NA |
| B.常温常压下,22.4 L二氧化碳含有的原子总数为3NA |
| C.1 mol Fe与足量稀HNO3反应,转移3 NA个电子 |
| D.1 L 1 mol·L-1的NaClO 溶液中含有ClO-的数目为NA |