题目内容
5.相同质量的铜片分别与体积相同且过量的浓硝酸、稀硝酸反应,二者比较相等的是( )| A. | 铜片消耗完所需时间 | |
| B. | 反应中氧化剂得到电子总数 | |
| C. | 反应后溶液中铜离子浓度(反应后溶液体积不变) | |
| D. | 反应生成气体的体积(同温、同压) |
分析 A、硝酸浓度不同反应速率不同;
B、铜与过量硝酸反应,硝酸得到电子等于铜失去的电子;
C、反应后铜离子物质的量相同,溶液体积相同,所以浓度相同;
D、铜和浓硝酸反应生成二氧化氮气体,和稀硝酸反应生成一氧化氮,铜失电子相同,生成气体不同体积不同.
解答 解:A、硝酸浓度不同反应速率不同,铜片消耗完所需时间不同,故A不符合;
B、铜与过量硝酸反应硝酸得到电子等于铜失去的电子,反应中氧化剂得到电子的总数相同;故B符合;
C、反应后铜离子物质的量相同,溶液体积相同,所以浓度相同,故C符合;
D、铜和浓硝酸反应生成二氧化氮气体,和稀硝酸反应生成一氧化氮,铜失电子相同,生成气体不同,体积不同,故D不符合;
故选BC.
点评 本题考查了硝酸性质,氧化还原反应电子转移计算分析判断,注意硝酸浓度不同生成气体不同,题目难度中等.

练习册系列答案
 走进文言文系列答案
走进文言文系列答案
相关题目
13.已知25℃时,电离常数Ka(HF)=3.6×10-4,溶度积常数Ksp(CaF2)=1.46×10-10现向1L0.2Lmol.L-1HF溶液中加入1L0.2Lmol.L-1CaCl2溶液,则下列说法中正确的是( )
| A. | 25℃时,0.1mol•L-1HF溶液中pH=1 | |
| B. | Ksp(CaF2)随温度和浓度的变化而变化 | |
| C. | 该体系中没有沉淀产生 | |
| D. | 该体系中有CaF2产生沉淀 |
20.以焦炭为主要原料合成NH3,为了使通入合成塔的N2与H2保持1:3的体积比,则焦炭(不计燃烧中的消耗)与空气的物质的量之比约为( )(N2约占空气总体积的$\frac{4}{5}$)
| A. | 1:3 | B. | 3:2 | C. | 6:5 | D. | 4:3 |
10.下列有机物的名称与结构简式相符的是( )
| A. | 石炭酸: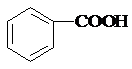 | B. | 甘油: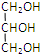 | C. | 蚁酸:CH3COOH | D. | 木精:CH3CH2OH |
17.下表为三种元素的性质或结构信息:下列推断正确的是( )
| 元素编号 | 元素性质或结构 |
| X | 3p亚层上有1个空轨道 |
| Y | 第三周期元素形成的简单离子中半径最大 |
| Z | 短周期中原子最容易失电子 |
| A. | 氢化物的稳定性:X<Y | B. | 单质与水反应的难易程度:Y>Z | ||
| C. | 单质的熔点:X<Y<Z | D. | X、Y、Z的氧化物晶体类型相同 |
14.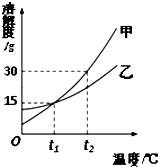 甲、乙两种固体的溶解度曲线如图所示,下列说法正确的是( )
甲、乙两种固体的溶解度曲线如图所示,下列说法正确的是( )
 甲、乙两种固体的溶解度曲线如图所示,下列说法正确的是( )
甲、乙两种固体的溶解度曲线如图所示,下列说法正确的是( )| A. | 甲的溶解度大于乙的溶解度 | |
| B. | 将甲的饱和溶液变为不饱和溶液可采用降温的方法 | |
| C. | t1℃时,甲、乙的饱和溶液中溶质的质量分数不一定相等 | |
| D. | t2℃时,将甲、乙等质量的饱和溶液降温至t1℃,甲析出的固体一定大于乙 |
15.下列实验设计不合理的是( )
| A. | 比较相同条件下水解能力:室温下用pH计分别测量同浓度的Na2CO3和NaHCO3溶液的pH | |
| B. | 检验乙烯:无水乙醇和浓硫酸共热到170℃,将制得的气体通入酸性高锰酸钾溶液,观察到溶液紫色很快褪去,证明反应生成了乙烯 | |
| C. | 检验铝热剂中铁的价态:将铝热剂溶于足量稀盐酸再滴加KSCN溶液,未出现血红色,证明该铝热剂不含氧化铁 | |
| D. | 在2mL同浓度的NaCl、NaI混合溶液中滴入几滴稀AgNO3溶液,观察到产生黄色沉淀,证明Ksp(AgCl)>Ksp(AgI) |
 ,B为18电子分子,其结构式为
,B为18电子分子,其结构式为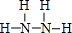 .
.