题目内容
【题目】中国政府承诺,到2020年,单位GDP二氧化碳排放比2005年下降40%~50%。CO2可转化成有机物实现碳循环。在体积为1L的密闭容器中,充入1molCO2和3molH2,一定条件下反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如图所示。
CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如图所示。

(1)从3min到9min,v(CO2)=__mol·L-1·min-1(计算结果保留2位有效数字)。
(2)能说明上述反应达到平衡状态的是__(填编号)。
A.反应中CO2与CH3OH的物质的量浓度之比为1∶1(即图中交叉点)
B.混合气体的压强不随时间的变化而变化
C.单位时间内生成1molH2,同时生成1molCH3OH
D.混合气体的平均相对分子质量不随时间的变化而变化
(3)平衡时CO2的转化率为__%。
(4)平衡混合气体中CO2(g)和H2(g)的质量之比是__。
(5)第3分钟时v正(CH3OH)__第9分钟时v逆(CH3OH)(填“>”、“<”“=”或“无法比较”)。
【答案】0.042 BD 75 22:3 >
【解析】
(1)3min到9min,根据CO2浓度变化计算CO2化学反应速率v(CO2);
(2)化学反应达到平衡状态时正逆反应速率相等,各物质的浓度不变,由此衍生的物理量不变;
(3)由图象可知平衡时CO2的为0.25mol/L,可知消耗0.75mol/L,以此计算转化率;
(4)结合各物质的平衡浓度,利用三段式法计算;
(5)第9分钟时达到平衡,υ逆(CH3OH)=υ正(CH3OH),随着反应的进行,正反应速率逐渐减小。
(1)3min到9min,CO2浓度变化为0.5mol/L0.25mol/L=0.25mol/L,CO2反应速率为:![]() ,故答案为:0.042;
,故答案为:0.042;
(2)A.反应中CO2与CH3OH的物质的量浓度之比为1:1(即图中交叉点),浓度相等而不是不变,故A错误;
B. 混合气体的物质的量为变量,则压强为变量,随着反应的进行,混合气体的压强不随时间的变化而变化,此时反应达到平衡,故B正确;
C. 单位时间内生成3molH2,同时生成1molCH3OH,则正逆反应速率相等,故C错误;
D.混合气体的质量不变,混合气体的物质的量随着反应的进行是变量,则平均相对分子质量不随时间的变化而变化此时反应达到平衡,故D正确;
故答案为:BD;
(3)由图象可知平衡时CO2的为0.25mol/L,可知消耗0.75mol/L,则转化率为![]() ,故答案为:75;
,故答案为:75;
(4)
则平衡时混合气体中CO2(g)和H2(g)的质量之比是![]() ,故答案为:22:3;
,故答案为:22:3;
(5)第9分钟时达到平衡,υ逆(CH3OH)=υ正(CH3OH),随着反应的进行,正反应速率逐渐减小,则第3分钟时υ正(CH3OH) 大于第9分钟时υ逆(CH3OH)。故答案为:>。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】铬元素有许多独特性质,如铬作为炼钢的添加料,可生产多种高强度、抗腐 蚀、耐磨、耐高温、耐氧化的特种钢;铬的化合物色彩众多,如 Cr3+(紫色)、Cr(OH)3(灰蓝色)、 CrO2(绿色)等。请回答下列问题:
Ⅰ.铬可形成 Cr(NO3)3、NaCrO2 等盐类物质,则 NaCrO2 中铬元素的化合价为_____,向Cr(NO3)3 溶液中滴加 NaOH 溶液至过量,可观察到的主要现象是_____。
Ⅱ.铬元素的+6 价化合物毒性较大,不能随意排放。某化工厂以铬渣(含有 Na2SO4 及少量Cr 2O72、Fe3+)为原料提取硫酸钠,同时制备金属铬的工艺流程如下:
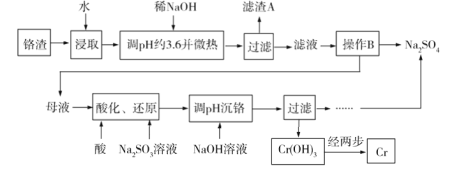
已知:金属离子生成氢氧化物沉淀的 pH 如下表所示:
氢氧化物 | Fe(OH)3 | Cr(OH)3 |
开始沉淀的 pH | 1.5 | 6 |
沉淀完全的 pH | 3.6 | 8 |
(1)滤渣 A 的主要成分为_____。
(2)根据下图信息,可知操作 B 包含蒸发结晶和_____。

(3)酸化后的 Cr2O72-可被 SO32-还原,该反应中若有 0.5 molCr2O72-被还原为 Cr3+ ,则消耗 SO32-的物质的量为_____mol。
(4)调 pH 沉铬步骤中,应调节 pH 的范围是_____(填字母)。
A.1.5~3.6 B.3.6~6 C.6~8 D.8~9
(5)通过两步反应可以实现Cr(OH)3转化为 Cr,第一步反应为2Cr(OH)3=Cr2O3+3H2O;第二步反应利用了铝热反应原理,则该步反应的化学方程式为_____。