题目内容
(12分)某化学兴趣小组同学进行如下实验。
(1)使用铜和稀硫酸制备硫酸铜晶体。步骤如下:
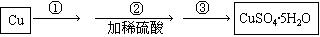
步骤①观察到的现象是: 。
步骤③的主要操作包括: 。
(2)某同学查资料知:铜与稀硫酸不反应,若在稀硫酸中加入H2O2,铜可逐渐溶解。实验装置如图,写出该反应的化学方程式: 。

(3)铜粉放入稀硫酸中,加热后无明显现象发生。当加入一种物质后,铜粉开始溶解,溶液变蓝色,同时有气体逸出,该物质是 (填字母);
写出该反应的离子方程式 。
(1)使用铜和稀硫酸制备硫酸铜晶体。步骤如下:

步骤①观察到的现象是: 。
步骤③的主要操作包括: 。
(2)某同学查资料知:铜与稀硫酸不反应,若在稀硫酸中加入H2O2,铜可逐渐溶解。实验装置如图,写出该反应的化学方程式: 。

(3)铜粉放入稀硫酸中,加热后无明显现象发生。当加入一种物质后,铜粉开始溶解,溶液变蓝色,同时有气体逸出,该物质是 (填字母);
| A.Al2(SO4)3 | B.Na2CO3 | C.KNO3 | D.FeSO4 |
(1)红色固体变黑(2分) 加热浓缩,冷却结晶,过滤。(3分)
(2)Cu + H2O2 + H2SO4= CuSO4 + 2H2O (3分)
(3)C (2分) 3Cu + 8H+ + 2NO3- =3Cu2+ + 4H2O + 2NO↑ (2分)
(2)Cu + H2O2 + H2SO4= CuSO4 + 2H2O (3分)
(3)C (2分) 3Cu + 8H+ + 2NO3- =3Cu2+ + 4H2O + 2NO↑ (2分)
(1)铜首先被氧气氧化为CuO,再加硫酸生成硫酸铜溶液,然后通过加热浓缩,冷却结晶,过滤来制取产物
(2)在酸性条件下铜被H2O2氧化
(3)在酸性条件下2NO3-可氧化铜单质。
(2)在酸性条件下铜被H2O2氧化
(3)在酸性条件下2NO3-可氧化铜单质。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目