题目内容
【题目】在一定条件下发生反应:3A(g)+ 2B(g)![]() xC(g)+2D(g),在 2L 的密闭容器中,把 4molA 和 2molB 混合,2min后达到平衡时生成 1.6molC,又测得反应速率 v(B)= 0.2mol·(L·min)-1,下列说法正确的是( )
xC(g)+2D(g),在 2L 的密闭容器中,把 4molA 和 2molB 混合,2min后达到平衡时生成 1.6molC,又测得反应速率 v(B)= 0.2mol·(L·min)-1,下列说法正确的是( )
A.A的平衡浓度是2.8mol·L-1B.B 的转化率是20%
C.x= 4D.平衡时气体压强是原来的 0.9倍
【答案】C
【解析】
根据题中3A(g)+ 2B(g)![]() xC(g)+2D(g)可知,本题考查化学反应速率计算,运用化学反应速率之比等于化学计量数之比和气体物质的量之比等于压强之比分析。
xC(g)+2D(g)可知,本题考查化学反应速率计算,运用化学反应速率之比等于化学计量数之比和气体物质的量之比等于压强之比分析。
根据反应速率之比等于化学计量数之比来确定化学计量数x,
v(B)= 0.2mol·(L·min)-1, 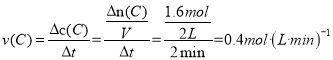 ,则x=4
,则x=4
则

A. A的平衡浓度是![]() ,A项错误;
,A项错误;
B.B的转化率=![]() ,B项错误;
,B项错误;
C.计算可知:x=4,C项正确;
D.气体物质的量之比等于压强之比,平衡时气体压强是原来的![]() ,D项错误;
,D项错误;
答案选C。

 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案【题目】实验室制备1,2-二溴乙烷,可用足量的乙醇先制备乙烯,再用乙烯和少量的溴制备1,2-二溴乙烷,装置如下图所示:
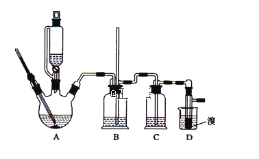
有关数据列表如下:
乙醇 | 1,2-二溴乙烷 | 乙醚 | |
状态 | 无色液体 | 无色液体 | 无色液体 |
密度/g · cm-3 | 0.79 | 2.2 | 0.71 |
沸点/℃ | 78.5 | 132 | 34.6 |
熔点/℃ | -130 | 9 | -116 |
回答下列问题:
(1)写出由乙醇制备乙烯的化学方程式______________________________,乙烯制备1,2-二溴乙烷的化学方程式_______________________________。
(2)在此制备实验中,要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是___________;(填正确选项前的字母)
a.引发反应 b.加快反应速度
c.防止乙醇挥发 d.减少副产物乙醚生成
(3)在装置A中除了浓硫酸和乙醇外,还应加入_____,其目的是_______装置A中生成副产物乙醚的化学反应方程式 ___________________。
(4)实验室制取乙烯,常因温度过高而使乙醇和浓H2SO4反应生成少量的二氧化硫,为了验证二氧化硫的存在并除去二氧化硫对后续反应的干扰,某同学在A和D之间加入了B、C两个装置,其中B和C中可分别盛放 ________________,
a.酸性KMnO4和水 b.品红和NaOH溶液
c.酸性KMnO4和NaOH溶液d.品红和酸性KMnO4
(5)将1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在_____层(填“上”、“下”);若产物中有少量副产物乙醚。可用_______的方法除去。
【题目】在3种不同条件下,分别向容积为2L的恒容密闭容器中充入2molA和1molB,发生反应:![]()
![]() 。相关条件和数据见下表:
。相关条件和数据见下表:
实验编号 | 实验Ⅰ | 实验Ⅱ | 实验Ⅲ |
反应温度/℃ | 700 | 700 | 750 |
达平衡时间/min | 40 | 5 | 30 |
n(D)平衡/mol | 1.5 | 1.5 | 1 |
化学平衡常数 | K1 | K2 | K3 |
下列说法正确的是( )
A. 实验Ⅲ达平衡后,恒温下再向容器中通入1molA和1molD,平衡不移动
B. 升高温度能加快反应速率的原理是降低了活化能,使活化分子百分数提高
C. 实验Ⅲ达平衡后容器内的压强是实验Ⅰ的0.9倍
D. K3>K2>K1