��Ŀ����
����������̼Ԫ�صĵ��ʺͻ�����Ӧ�ù㷺������Ԫ�صĵ��ʼ������������ʵ������ת����
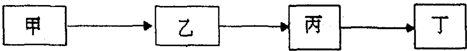
������ÿ��ת��ʱ�ס��ҡ�����������������ֻ��һ���ǵ��ʣ������������о�������ɸõ��ʵ�Ԫ�أ���ش�
��1�������ǵؿ��к������Ľ���Ԫ�صĵ��ʣ���������ˮ����Һ�Լ��ԣ�������������ӷ���ʽ��______��
��2��������һ�ֳ������������壬��ͬ�����£����Ͷ�����Һ���Լ��ԣ��ұ�����Һ�ļ���ǿ�ڶ�����Һ�ļ��ԣ��ҵ��������ӷ���ʽ��______��
��3���������д��Եĺ�ɫ���壬�����м���ϡ�����ɵõ�����ͬʱ�õ�һ����ɫ���壬�������������ʺ���ɫ���÷�Ӧ�Ļ�ѧ����ʽ��______��
��4���ڼ���п����У��ø��������Ϊ�������ϣ���ط�ӦΪ��2K2FeO4+3Zn=Fe2O3+ZnO+2K2ZnO2�õ�����������ķ�Ӧ�ĵ缫��ӦʽΪ______��
����������п��غͶ��Ե缫���1000mL1mol/L��AgNO3��Һ�����ص��ܷ�Ӧ����ʽΪ______�����������0.05molZnʱ���������Һ��pHΪ______����Һ����仯���Բ��ƣ���
��5����ȡ�����ơ���������mg���������·ֱ���VL4mol?L-1�������ַ�Ӧ�����ж���������������£�Vֵ��ȡֵ��Χ���ú�m�ı���ʽ��ʾ����
���������ᷴӦ�ų���������ࣺ______��
���������ᷴӦ�ų���������ࣺ______��

������ÿ��ת��ʱ�ס��ҡ�����������������ֻ��һ���ǵ��ʣ������������о�������ɸõ��ʵ�Ԫ�أ���ش�
��1�������ǵؿ��к������Ľ���Ԫ�صĵ��ʣ���������ˮ����Һ�Լ��ԣ�������������ӷ���ʽ��______��
��2��������һ�ֳ������������壬��ͬ�����£����Ͷ�����Һ���Լ��ԣ��ұ�����Һ�ļ���ǿ�ڶ�����Һ�ļ��ԣ��ҵ��������ӷ���ʽ��______��
��3���������д��Եĺ�ɫ���壬�����м���ϡ�����ɵõ�����ͬʱ�õ�һ����ɫ���壬�������������ʺ���ɫ���÷�Ӧ�Ļ�ѧ����ʽ��______��
��4���ڼ���п����У��ø��������Ϊ�������ϣ���ط�ӦΪ��2K2FeO4+3Zn=Fe2O3+ZnO+2K2ZnO2�õ�����������ķ�Ӧ�ĵ缫��ӦʽΪ______��
����������п��غͶ��Ե缫���1000mL1mol/L��AgNO3��Һ�����ص��ܷ�Ӧ����ʽΪ______�����������0.05molZnʱ���������Һ��pHΪ______����Һ����仯���Բ��ƣ���
��5����ȡ�����ơ���������mg���������·ֱ���VL4mol?L-1�������ַ�Ӧ�����ж���������������£�Vֵ��ȡֵ��Χ���ú�m�ı���ʽ��ʾ����
���������ᷴӦ�ų���������ࣺ______��
���������ᷴӦ�ų���������ࣺ______��
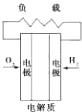
��1�������ǵؿ��к������Ľ���Ԫ�صĵ��ʣ��жϱ�ΪAl����������ˮ����Һ�Լ��ԣ��ж�Ϊ���ͼӦ���ɵ�ƫ��������Һ�����ΪAl��OH��3����ΪAl2O3�����Ͷ���Ӧ�����ӷ���ʽΪ��2Al+2OH-+2H2O=2AlO2-+3H2����
�ʴ�Ϊ��2Al+2OH-+2H2O=2AlO2-+3H2����
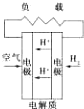
��2��������һ�ֳ������������壬�ж�ΪCO2����ͬ�����£����Ͷ�����Һ���Լ��ԣ��ұ�����Һ�ļ���ǿ�ڶ�����Һ�ļ��ԣ��ƶ�Ϊ��ΪNa2CO3����ΪNaHCO3���ҵ��������ӷ���ʽ�Ƕ�����̼���������Ʒ�Ӧ�����ӷ�ӦΪ��CO2+2OH-=CO32-+H2O��
�ʴ�Ϊ��CO2+2OH-=CO32-+H2O��
��3���������д��Եĺ�ɫ���壬�ж�ΪFe3O4�������м���ϡ���������������������Ϊ�����ӣ��ɵõ�����������ͬʱ�õ�һ����ɫ����NO���������������ʺ���ɫNO2���÷�Ӧ�Ļ�ѧ����ʽ�ǣ�3Fe3O4+28HNO3��ϡ��=9Fe��NO3��3+NO��+14H2O��
�ʴ�Ϊ��3Fe3O4+28HNO3��ϡ��=9Fe��NO3��3+NO��+14H2O��
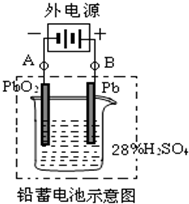
��3���ڼ���п����У��ø��������Ϊ�������ϣ���ط�ӦΪ��2K2FeO4+3Zn=Fe2O3+ZnO+2K2ZnO2�õ�����������ķ�Ӧ�ĵ缫��Ӧʽ���ݸ�����صõ����ӷ�����ԭ��Ӧ��������������д��������غ�����������������ƽ�õ������缫��ӦΪ��2FeO42-+6e-+5H2O=Fe2O3+10OH-������������п��غͶ��Ե缫���1000mL1mol/L��AgNO3��Һ�����ص��ܷ�Ӧ����ʽΪ��4AgNO3+2H2O
4Ag+O2��+4HNO3�����������0.05molZnʱ����ת��Ϊ0.1mol�������ݻ�ѧ����ʽ���㣬ת��4mol��������4mol�����ӣ�����ת��0.1mol�����������������ʵ���Ϊ0.1mol��������Ũ��Ϊ0.1mol/L����ҺpH=1��
�ʴ�Ϊ��2FeO42-+6e-+5H2O=Fe2O3+10OH-��4AgNO3+2H2O
4Ag+O2��+4HNO3��1��
��5����ȡ�����ơ���������m g���������·ֱ���V L 4mol?L-1�������ַ�Ӧ�����ж���������������£�Vֵ��ȡֵ��Χ���ݽ��������ᷴӦ�Ķ�����ϵ�����жϣ��������ȫ����Ӧʱ�Ķ�����ϵΪ��
2Na��2HCl��H2
Fe��2HCl��H2
2Al��6HCl��3H2
���ݶ���������֪��
���������ᷴӦ�ų����������ʱ��������ƹ������������ǡ�÷�Ӧ���㣬���ĵ���������4V��
��V��
���ʴ�Ϊ��V��
��
���������ᷴӦ�ų����������ʱ�����������ᶼ�����������Ƽ�����Ҫ�����������4V��
��V��
���ʴ�Ϊ��0��V��
��
�ʴ�Ϊ��2Al+2OH-+2H2O=2AlO2-+3H2����
��2��������һ�ֳ������������壬�ж�ΪCO2����ͬ�����£����Ͷ�����Һ���Լ��ԣ��ұ�����Һ�ļ���ǿ�ڶ�����Һ�ļ��ԣ��ƶ�Ϊ��ΪNa2CO3����ΪNaHCO3���ҵ��������ӷ���ʽ�Ƕ�����̼���������Ʒ�Ӧ�����ӷ�ӦΪ��CO2+2OH-=CO32-+H2O��
�ʴ�Ϊ��CO2+2OH-=CO32-+H2O��
��3���������д��Եĺ�ɫ���壬�ж�ΪFe3O4�������м���ϡ���������������������Ϊ�����ӣ��ɵõ�����������ͬʱ�õ�һ����ɫ����NO���������������ʺ���ɫNO2���÷�Ӧ�Ļ�ѧ����ʽ�ǣ�3Fe3O4+28HNO3��ϡ��=9Fe��NO3��3+NO��+14H2O��
�ʴ�Ϊ��3Fe3O4+28HNO3��ϡ��=9Fe��NO3��3+NO��+14H2O��
��3���ڼ���п����У��ø��������Ϊ�������ϣ���ط�ӦΪ��2K2FeO4+3Zn=Fe2O3+ZnO+2K2ZnO2�õ�����������ķ�Ӧ�ĵ缫��Ӧʽ���ݸ�����صõ����ӷ�����ԭ��Ӧ��������������д��������غ�����������������ƽ�õ������缫��ӦΪ��2FeO42-+6e-+5H2O=Fe2O3+10OH-������������п��غͶ��Ե缫���1000mL1mol/L��AgNO3��Һ�����ص��ܷ�Ӧ����ʽΪ��4AgNO3+2H2O
| ||
�ʴ�Ϊ��2FeO42-+6e-+5H2O=Fe2O3+10OH-��4AgNO3+2H2O
| ||
��5����ȡ�����ơ���������m g���������·ֱ���V L 4mol?L-1�������ַ�Ӧ�����ж���������������£�Vֵ��ȡֵ��Χ���ݽ��������ᷴӦ�Ķ�����ϵ�����жϣ��������ȫ����Ӧʱ�Ķ�����ϵΪ��
2Na��2HCl��H2
| m |
| 23 |
| m |
| 23 |
| m |
| 46 |
Fe��2HCl��H2
| m |
| 56 |
| m |
| 28 |
| m |
| 56 |
2Al��6HCl��3H2
| m |
| 27 |
| m |
| 9 |
| m |
| 18 |
���ݶ���������֪��
���������ᷴӦ�ų����������ʱ��������ƹ������������ǡ�÷�Ӧ���㣬���ĵ���������4V��
| m |
| 23 |
| m |
| 92 |
| m |
| 92 |
���������ᷴӦ�ų����������ʱ�����������ᶼ�����������Ƽ�����Ҫ�����������4V��
| m |
| 23 |
| m |
| 92 |
| m |
| 92 |

��ϰ��ϵ�д�
 ������ÿ�ʱ��ҵϵ�д�
������ÿ�ʱ��ҵϵ�д�
�����Ŀ
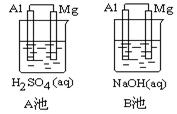
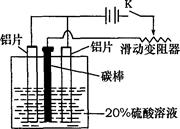
 ��
��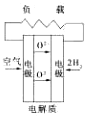
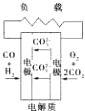
 2CO2��N2��H��0����÷�Ӧһ�����Է�����
2CO2��N2��H��0����÷�Ӧһ�����Է����� 2NH3(g)��������������ʱ����N2�����淴Ӧ���ʾ�����
2NH3(g)��������������ʱ����N2�����淴Ӧ���ʾ�����