题目内容
3.FeCl3在现代工业生产中应用广泛.某化学研究性学习小组模拟工业生产流程制备无水FeCl3,再用副产品FeCl3溶液吸收有毒的H2S.经查阅资料得知:无水FeCl3在空气中易潮解,加热易升华.他们设计了制备无水FeCl3的实验方案,装置示意图(加热及夹持装置略去)及操作步骤如下:
①检查装置的气密性;
②通入干燥的Cl2,赶尽装置中的空气;
③用酒精灯在铁屑下方加热至反应完成
④…
⑤体系冷却后,停止通入Cl2,并用干燥的N2赶尽Cl2,将收集器密封
请回答下列问题:
(1)写出FeCl3溶液吸收有毒的H2S的离子方程式为2Fe3++H2S=2Fe2++S↓+2H+.
(2)第③步加热后,生成的烟状FeCl3大部分进入收集器,少量沉积在反应管A的右端.要使沉积得FeCl3进入收集器,第④步操作是在沉积的FeCl3固体下方加热.
(3)操作步骤中,为防止FeCl3潮解所采取的措施有(填步骤序号)②⑤.
(4)装置B中的冷水作用为冷却FeCl3使其沉积,便于收集产品;装置C的名称为干燥管;装置D中FeCl2全部反应完后,因为失去吸收Cl2的作用而失效,从下面选出检验FeCl2是否完全失效的试剂:B.
A.氢氧化钠溶液 B.酸性高锰酸钾溶液 C.硫氰化钾溶液 D.氨水
(5)在虚线框内画出尾气吸收装置E并注明试剂.
分析 (1)FeCl3溶液吸收有毒的H2S发生氧化还原反应生成硫单质,氯化亚铁和盐酸;
(2)要使沉积的FeCl3进入收集器,根据FeCl3加热易升华的性质;
(3)防止FeCl3潮解,不与水蒸气接触;
(4)B中的冷水作用为是冷却FeCl3使其沉积,便于收集产品;装置C的名称为干燥管;检验FeCl2是否失效应检验FeCl2是否存在,可以用KMnO4溶液检验;
(5)用氢氧化钠溶液吸收的是氯气,不用考虑防倒吸.
解答 解:(1)FeCl3溶液吸收有毒的H2S发生氧化还原反应生成硫单质,氯化亚铁和盐酸,反应的离子方程式为:2Fe3++H2S=2Fe2++S↓+2H+,
故答案为:2Fe3++H2S=2Fe2++S↓+2H+;
(2)对FeCl3加热发生升华使沉积的FeCl3进入收集器,故答案为:在沉积的FeCl3固体下方加热;
(3)为防止FeCl3潮解所采取的措施有②通入干燥的Cl2⑤用干燥的N2赶尽Cl2,故选:②⑤,
故答案为:②⑤;
(4)B中的冷水作用为是冷却FeCl3使其沉积,便于收集产品,装置C的名称为干燥管;
检验FeCl2是否失效应检验FeCl2是否存在,可以用KMnO4溶液检验;
故答案为:冷却,使FeCl3沉积,便于收集产品;干燥管;B;
(5)用氢氧化钠溶液吸收的是氯气,不用考虑防倒吸,故答案为: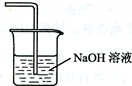 .
.
点评 本题是一道综合题,难度中等,考查了学生运用知识解决问题的能力,涉及到的知识点较多,掌握基础是关键.

练习册系列答案
相关题目
2.请选用适当的试剂和分离方法除去下列物质中所含的杂质(括号内为杂质),将所选的试剂及分离方法的编号填入表中.
试剂:a.H2O b.酸性KMnO4溶液 c.Br2的CCl4溶液 d.饱和Na2CO3溶液 e.新制CaO
分离方法:A.分液 B.过滤 C.洗气 D.蒸馏 E.盐析
试剂:a.H2O b.酸性KMnO4溶液 c.Br2的CCl4溶液 d.饱和Na2CO3溶液 e.新制CaO
分离方法:A.分液 B.过滤 C.洗气 D.蒸馏 E.盐析
| 混合物 | 选择试剂 | 分离方法 |
| 二氧化硫(乙烯) | c | C |
| 乙醇(水) | e | D |
| 乙酸乙酯(乙酸) | d | A |
3.某混合溶液中含SO42-0.25mol/L,含Cl-0.5mol/L,NO3-0.25mol/L,含Na+0.25mol/L,其余为H+,则H+的物质的量浓度为( )
| A. | 5mol/L | B. | 2.5mol/L | C. | 1mol/L | D. | 0.1mol/L |
8. 冬青油是天然香料之一,其主要成分为水杨酸甲酯,可由水杨酸(邻羟基苯甲酸)和甲醇作原料在浓硫酸催化下酯化而得.
冬青油是天然香料之一,其主要成分为水杨酸甲酯,可由水杨酸(邻羟基苯甲酸)和甲醇作原料在浓硫酸催化下酯化而得.
实验步骤:
Ⅰ.如图,在100mL三口烧瓶中放入6.9g(0.05mol)水杨酸和24g(30mL,0.75mol)甲醇,向混合物中加入约10mL甲苯,再小心地加入8mL浓硫酸,摇动混匀:加入1~2粒沸石,装上回流冷凝管在石棉网上保持85-95℃,加热回流1.5-2小时:
Ⅱ.待装置冷却后,分离出甲醇,向烧瓶中加入50mL,水,然后转移至分液漏斗,分出下层产物,弃去上层水层,有机层再倒入分液漏斗中;依次用50mL 5% NaHCO3溶液洗1次(溶液呈弱碱性),30mL水洗一次(产物皆在下层),有机层得到粗酯;
Ⅲ.将粗酯进行蒸馏,收集221℃~224℃的馏分.产品经0.5g无水CaCl2干燥后称重.
已知:甲苯与水形成的共沸物,沸点为85℃,该实验中加入甲苯,易将水蒸出.
常用物理常数:
请根据以上信息回答下列问题:
(1)制备冬青油的化学方程式为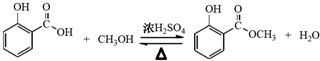 ;.
;.
(2)制备冬青油时,最合适的加热方法是水浴加热.实验中加入甲苯作带水剂的目的是反应产生的水从反应体系中分离开来,使得平衡向右移动,同时可以减少甲醇的用量,从而提高反应的产率.
(3)反应结束冷却后,分离甲醇的操作是:蒸馏;
(4)在提纯粗产品的过程中,用碳酸氢钠溶液洗涤主要除去的杂质是水杨酸:若改用氢氧化钠溶液是否可以不可以(填“可以”或“不可以”),其原因是在氢氧化钠溶液中水杨酸甲酯发生水解.
(5)检验产品中是否含有水杨酸的化学方法是取少量晶体于试管中,加蒸馏水溶解,滴加NaHCO3溶液,若出现无色气泡则含水杨酸.最终称得产品的质量为4.2g,则所得水杨酸甲酯的产率为55%(保留两位有效数字).
 冬青油是天然香料之一,其主要成分为水杨酸甲酯,可由水杨酸(邻羟基苯甲酸)和甲醇作原料在浓硫酸催化下酯化而得.
冬青油是天然香料之一,其主要成分为水杨酸甲酯,可由水杨酸(邻羟基苯甲酸)和甲醇作原料在浓硫酸催化下酯化而得.实验步骤:
Ⅰ.如图,在100mL三口烧瓶中放入6.9g(0.05mol)水杨酸和24g(30mL,0.75mol)甲醇,向混合物中加入约10mL甲苯,再小心地加入8mL浓硫酸,摇动混匀:加入1~2粒沸石,装上回流冷凝管在石棉网上保持85-95℃,加热回流1.5-2小时:
Ⅱ.待装置冷却后,分离出甲醇,向烧瓶中加入50mL,水,然后转移至分液漏斗,分出下层产物,弃去上层水层,有机层再倒入分液漏斗中;依次用50mL 5% NaHCO3溶液洗1次(溶液呈弱碱性),30mL水洗一次(产物皆在下层),有机层得到粗酯;
Ⅲ.将粗酯进行蒸馏,收集221℃~224℃的馏分.产品经0.5g无水CaCl2干燥后称重.
已知:甲苯与水形成的共沸物,沸点为85℃,该实验中加入甲苯,易将水蒸出.
常用物理常数:
| 名称 | 相对分子质量 | 相对密度 | 熔点(℃) | 沸点(℃) | 溶解度 |
| 水杨酸甲酯 | 152 | 1.5369 | -8.6 | 223.3 | 微溶 |
| 水杨酸 | 138 | 1.44 | 157 | 211 | 1.5g/L |
| 甲醇 | 32 | 0.79 | -97.8 | 64.5 | 混溶 |
(1)制备冬青油的化学方程式为
 ;.
;.(2)制备冬青油时,最合适的加热方法是水浴加热.实验中加入甲苯作带水剂的目的是反应产生的水从反应体系中分离开来,使得平衡向右移动,同时可以减少甲醇的用量,从而提高反应的产率.
(3)反应结束冷却后,分离甲醇的操作是:蒸馏;
(4)在提纯粗产品的过程中,用碳酸氢钠溶液洗涤主要除去的杂质是水杨酸:若改用氢氧化钠溶液是否可以不可以(填“可以”或“不可以”),其原因是在氢氧化钠溶液中水杨酸甲酯发生水解.
(5)检验产品中是否含有水杨酸的化学方法是取少量晶体于试管中,加蒸馏水溶解,滴加NaHCO3溶液,若出现无色气泡则含水杨酸.最终称得产品的质量为4.2g,则所得水杨酸甲酯的产率为55%(保留两位有效数字).
15.根据国家标准.含CrO${\;}_{4}^{2-}$的废水要经化学处理,使其浓度降至5.0×10-7mol.L-1以下才能排放,常用方法为:向废水中加人可溶性钡盐生成BaCrO4沉淀.再加人某种试剂处理多余的Ba2+[已知:Ksp(BaCrO4)=1.2×10-10溶于酸碱],下列说法不正确的是( )
| A. | 含CrOi${\;}_{4}^{2-}$、Ba2+的废水属于重金属污染 | |
| B. | 从物质分类的角度看.除去多余的Ba2+.所加的试剂类型为硫酸盐 | |
| C. | 加入可溶性钡盐后,废水中人可溶性沏盐后,废水中Ba〃的浓度应不小于2+的浓度应不小于2.4×10-2mol.L-1 | |
| D. | BaCrO4与碳酸钙类似均属于电解质 |
12.25℃时,将某一元碱MOH和盐酸溶液等体积混合(体积变 化忽略不计),测得反应后溶液的pH如下表,则下列判断不正确的是( )
| 实验编号 | c(盐酸)/(mol/L) | c(MOH)/(mol/L) | 反应后溶液的pH |
| 甲 | 0.20 | 0.20 | 5 |
| 乙 | 0.10 | a | 7 |
| A. | 实验甲所得溶液:c(Cl-)>c(M+)>c(H+)>c(MOH) | |
| B. | 将实验甲中所得溶液加水稀释后,$\frac{c({H}^{+})}{c({M}^{+})}$变小 | |
| C. | a>0.10 | |
| D. | MOH的电离平衡常数可以表示为Kb=$\frac{1{0}^{-8}}{a-0.10}$ |
13.元素R的最高价含氧酸的化学式为HnRO2n-2,则在其最低价气态氢化物中,R元素的化合价为( )
| A. | -10+3n | B. | -6+3n | C. | -12+3n | D. | -4+2n |