题目内容
常温下,柠檬水溶液的PH是3,其中的C(OH—)是 ( )
| A.0.1mol/L | B.1.0×10-3 mol/L | C.1.0×10-11mol/L | D.1.0×10-7mol/L |
C
c(H+)=10-3mol/L;c(OH-)=Kw/c(H+)=10-14/10-3=10-11mol/L;故答案为C。

练习册系列答案
相关题目
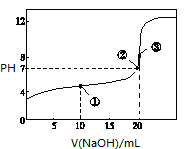
 .30mol/LCH3COOH水溶液 ⑤50毫升0.20mol/L蔗糖水溶液。以上各瓶溶液所含离子、分子总数的大小顺序是__________ _。
.30mol/LCH3COOH水溶液 ⑤50毫升0.20mol/L蔗糖水溶液。以上各瓶溶液所含离子、分子总数的大小顺序是__________ _。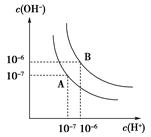

 。
。 =10-2mol·L-1
=10-2mol·L-1