题目内容
已知某温度下,0.l mol·L-1NaHB溶液中,C(H+)>c(OH-),则下列各关系式一定正确的是
| A.c(Na+)=c(HB-)+2c(B2-)+c(OH-) |
| B.溶液的pH="1" |
| C.c(Na+)="0.l" mol·L-1≥c(B2-) |
| D.C(H+).c(OH-)=10-14 |
C
A.根据题意,NaHB是强电解质,溶液呈酸性,如果存在HB-,则 HB-的电离程度大于水解程度,即 NaHB溶液中含有的离子是(Na+)、(H+)、c(HB-)、c(B2-)、c(OH-),根据电荷守恒得:c(Na+)+c(H+)=c(HB-)+2c(B2-)+c(OH-),故A错误;
B.NaHB是强电解质,溶液呈酸性,可能有两种情况,即HB-能够完全电离,也可能部分电离.当HB-完全电离时,0.1mol/L的NaHB的pH=1,当HB-部分电离时,0.1mol/L的NaHB的pH>1.故B错误;
C.NaHB是强电解质,说明0.1mol/L的NaHB的溶液中c(Na+)=0.1mol/L.根据B项的分析,当HB-完全电离时,0.1mol/L的NaHB的c(B2-)=0.1mol/L,当HB-部分电离时,c(B2-)<0.1mol/L.因此,c(Na+)=0.1mol/L≥c(B2-),故C正确;
D.在0.1mol/L的NaHB溶液中,无法求解氢离子的浓度,因而无法确定c(H+)-c(OH-)=10-14,但是可以知道c(H+)×c(OH-)=10-14,故D错误;
故选C.

练习册系列答案
 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案
相关题目
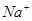
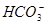
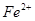
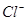
 变化的判断中,错误的是
变化的判断中,错误的是