题目内容
19.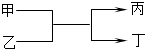 若甲、丙为短周期、同一主族元素组成的单质,乙、丁都是由两种元素组成的化合物,它们之间有如图所示的转化关系,则满足条件的甲和丙可以为( )
若甲、丙为短周期、同一主族元素组成的单质,乙、丁都是由两种元素组成的化合物,它们之间有如图所示的转化关系,则满足条件的甲和丙可以为( )| A. | 钠和氢气 | B. | 氟和氧气 | C. | 碳和硅 | D. | 氯气和溴 |
分析 若甲、丙为短周期、同一主族元素形成的单质,乙、丁都是由两种元素组成的化合物,该反应为置换反应,钠能和水或酸反应生成氢气、氟能和水反应生成氧气、碳和二氧化硅反应生成Si单质,溴属于长周期元素,据此分析解答.
解答 解:若甲、丙为短周期、同一主族元素形成的单质,乙、丁都是由两种元素组成的化合物,该反应为置换反应.
A.钠能和水或酸反应生成氢氧化钠和氢气、氢氧化钠含有3种元素,故A错误;
B.氟能和水反应生成氧气,F和O属于同一周期元素,故B错误;
C.碳和二氧化硅反应生成Si单质,且C和Si都属于同一主族短周期元素,符合条件,故C正确;
D.氯气和溴化钠反应生成溴单质,溴属于长周期元素,不符合条件,故D错误.
故选C.
点评 本题以元素化合物知识为载体考查置换反应及元素周期表结构等知识点,明确物质的性质是解本题关键,注意C能置换出Si单质,但生成CO而不是二氧化碳,为易错点.

练习册系列答案
相关题目
3.CaC2和ZnC2、Al4C3、Mg2C3、Li2C2等都同属离子型碳化物.请通过对CaC2制C2H2的反应进行思考,从中得到必要的启示,判断下列反应产物正确的是( )
| A. | ZnC2水解生成乙烷(C2H6 ) | B. | Al4C3水解生成丙炔(C3H4) | ||
| C. | Mg2C3水解生成丙炔(C3H4) | D. | Li2C2水解生成乙烯(C2H4) |
7.下列各组微粒半径的排列顺序正确的是( )
| A. | Na<Si<P | B. | O2->Mg2+>Al3+ | C. | Ca>Ba>Ca2+ | D. | Cl->F>F- |
14.下列四种元素中,其单质氧化性最强的是( )
| A. | 原子含有未成对电子最多的第二周期元素 | |
| B. | 位于元素周期表中第三周期ⅢA族的元素 | |
| C. | 原子最外层电子排布为2s22p6的元素 | |
| D. | 原子最外层电子排布为2s22p5的元素 |
11.下列变化中可以说明SO2具有漂白性的是( )
| A. | 通入酸性高锰酸钾溶液中红色褪去 | |
| B. | 通入品红溶液中红色褪去 | |
| C. | 通入溴水中橙黄色褪去 | |
| D. | 通入氢氧化钠的酚酞溶液中红色褪去 |

 .
.
 .
. .
. 的系统命名是:2,6-二甲基辛烷;
的系统命名是:2,6-二甲基辛烷;