题目内容
7.下列离子方程式正确的是( )| A. | 向稀硝酸中滴加Na2SO3溶液:SO32-+2H+═SO2↑+H2O | |
| B. | 氯气通入NaOH溶液中:Cl2+2OH-═Cl-+ClO-+H2O | |
| C. | 向Al2(SO4)3溶液中加入过量NH3•H2O:Al3++4NH3•H2O═AlO22-+4NH4++2H2O | |
| D. | 向水中加入Na2O2:Na2O2+H2O═2Na++2OH-+O2↑ |
分析 A.硝酸能够氧化亚硫酸根离子;
B.反应生成氯化钠、次氯酸钠和水;
C.不符合反应客观事实;
D.原子个数不守恒.
解答 解:A.向稀硝酸中滴加Na2SO3溶液,反应的离子方程式为:3SO32-+2NO3-+2H+═3SO42-+H2O+2NO↑,故A错误;
B.氯气通入NaOH溶液中,反应生成氯化钠、次氯酸钠和水,离子方程式:Cl2+2OH-═Cl-+ClO-+H2O,故B 正确;
C.向Al2(SO4)3溶液中加入过量NH3•H2O,反应生成产物为氢氧化铝,离子方程式:Al3++3NH3•H2O=Al(OH)3↓+3NH4+,故C错误;
D.过氧化钠与水反应离子方程式:N2a2O2+2H2O═4Na++4OH-+O2↑,故D错误;
故选:B.
点评 本题考查了离子方程式的书写,明确反应实质是解题关键,注意化学式的拆分、注意反应必须遵循客观事实,题目难度不大.

练习册系列答案
相关题目
17.下列有关说法正确的是( )
| A. | 在潮湿的环境中,铜容易发生析氢腐蚀形成铜绿 | |
| B. | 常温下,PH均为5的盐酸、氯化铵溶液中,水的电离程度相同 | |
| C. | 8NH3(g)+6NO(g)═7N2(g)+12H2O(g)△H<0,则该反应一定能自发进行 | |
| D. | 对于乙酸乙酯的水解反应(△H>0)加入少量氢氧化钠溶液并加热,该反应的反应速率和平衡常数均减小 |
18.下列关于氧化还原反应的说法不正确的是( )
| A. | 氧化还远反应的实质是电子的转移 | |
| B. | 含最高价元素的化合物均具有强氧化性 | |
| C. | 一定存在元素化合价的变化 | |
| D. | 氧化剂和还原剂混合不一定发生氧化还原反应 |
15.短周期元素X、Y、Z、W的原子序数依次增大,X与Z同主族,Y与W同主族,X的原子半径小于Y的原子半径,且X、Y、Z、W四种原子的最外层电子数之和为14.下列叙述正确的是( )
| A. | X和Z都是金属元素 | B. | X和Y只能结合形成一种化合物 | ||
| C. | W的最高化合价为+6 | D. | Z的单质不能与Y的单质反应 |
2.乙烯发生的下列反应中,不属于加成反应的是( )
| A. | 与水反应生成乙醇 | B. | 与溴水反应使之褪色 | ||
| C. | 与氢气反应生成乙烷 | D. | 与氧气反应生成二氧化碳和水 |
19.下列物质中,不是石油分馏产品的是( )
| A. | 石蜡油 | B. | 煤油 | C. | 润滑油 | D. | 色拉油 |
16.下列化学用语使用正确的是( )
| A. | F- 结构示意图: | |
| B. | 氯化钠的电子式: | |
| C. | 乙烯的结构简式:CH2=CH2 | |
| D. | 硫酸铁的电离方程式:Fe2(SO4)3=Fe23++3SO42- |
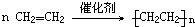 ;
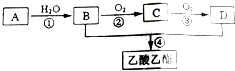
;
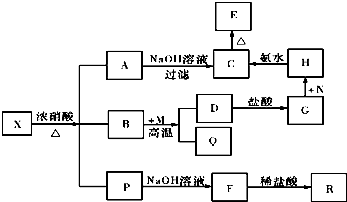
 X的化学式为Fe3C,P中气体的化学式为CO2、NO2.
X的化学式为Fe3C,P中气体的化学式为CO2、NO2.