��Ŀ����
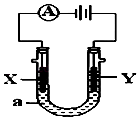
����Ŀ����ͼ��ʾ���Իش��������� �����ݹ��ʺ��ʣ���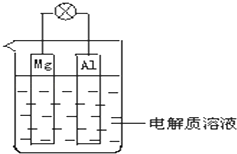
��1����װ�������ԭ��ء����ء�����
��2���������ҺΪϡH2SO4ʱ��Mg�缫Ϊ����Al�缫Ϊ����������������������缫�������������Һ��SO ![]() ��������ҡ����ƶ���Mg�缫�Ϸ����ķ�ӦΪ��Al�缫�Ϸ����ķ�ӦΪ��
��������ҡ����ƶ���Mg�缫�Ϸ����ķ�ӦΪ��Al�缫�Ϸ����ķ�ӦΪ��
��3���������ҺΪNaOH��aq��ʱ����Mg�缫Ϊ����Al�缫Ϊ��������������������������缫�������������Һ���������ӷ��ţ������ƶ���Mg�缫�Ϸ����ķ�ӦΪ�� �� Al�缫�Ϸ����ķ�ӦΪ�� ��
���𰸡�
��1��ԭ���
��2����������þ����Mg��2e��=Mg2+��2H++2e��=H2��
��3�������������������ӣ�2H2O+2e��=H2��+2OH����Al��3e��+4OH��=AlO ![]() +H2O
+H2O
���������⣺��1����װ���ǻ�ѧ��ת��Ϊ���ܣ����Ը�װ����ԭ��أ����Դ��ǣ�ԭ��أ���2���������ҺΪϡH2SO4ʱ��þ����������ϡ������Һ���γ�ԭ��أ���·���е������ɣ���������þ������ʧ��������þ���ӣ��缫��ӦΪ��Mg��2e��=Mg2+��������������Һ�������������缫�ϵõ����������������缫��ӦʽΪ��2H++2e��=H2�������Դ��ǣ���������þ����Mg��2e��=Mg2+��2H++2e��=H2������3���������ҺΪNaOH��Һʱ��þ��������������������Һ���γ�ԭ��أ���·���γɵ���������������������ʧ����������������Һ������ƫ��������Һ���缫��ӦΪ��Al��3e��+4OH��=AlO ![]() +H2O��þ����������Һ��ˮ�õ����������������缫��ӦʽΪ��2H2O+2e��=H2��+2OH�� �� ���Դ��ǣ������������������ӣ�2H2O+2e��=H2��+2OH����Al��3e��+4OH��=AlO
+H2O��þ����������Һ��ˮ�õ����������������缫��ӦʽΪ��2H2O+2e��=H2��+2OH�� �� ���Դ��ǣ������������������ӣ�2H2O+2e��=H2��+2OH����Al��3e��+4OH��=AlO ![]() +H2O��
+H2O��

 ��˼ά������ҵ���ټ��ִ�ѧ������ϵ�д�
��˼ά������ҵ���ټ��ִ�ѧ������ϵ�д�