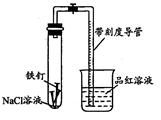
题目内容
甲醇可作为燃料电池的原料。以CH4和H2O为原料,通过下列反应来制备甲醇。
I:CH4(g)+H2O(g) CO(g)+3H2(g) △H=+206.0kJ?molˉ1
CO(g)+3H2(g) △H=+206.0kJ?molˉ1
II:CO(g)+2H2(g) CH3OH(g) △H=-129.0kJ?molˉ1
CH3OH(g) △H=-129.0kJ?molˉ1
(1)CH4(g)与H2O(g)反应生成CH3OH(g)和H2(g)的热化学方程式为 。
(2)将1.0mol CH4和1.0mol H2O(g)通入容积为100 L的反应室,在一定条件下发生反应I,测得在一定的压强下CH4的转化率与温度的关系如图。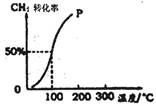
①假设100℃时达到平衡所需构时间为5min,则用H2表示该反应的平均反应速率为 。
②1000C时反应I的平衡常数为 。
(3)在压强为0.1 MPa、温度为300℃条件下,将a molCO与2a mol H2的混合气体在催化剂作用下发生反应II生成甲醇,平衡后将容器舶容积压缩到原来的1/2,其他条件不变,对平衡体系产生的影响是 (填字母序号)。
| A.平衡常数K增大 | B.正反应速率加快,逆反应速率减慢 |
| C.CH3OH的物质的量增加 | D.重新平衡c(H2)/c(CH3OH)减小 |
(16分)(1)CH4(g)+ H2O(g) CH3OH(g)+H2(g) △H=+77.0kJ?molˉ1(3分,焓变写错扣1分,用等号不扣分)
CH3OH(g)+H2(g) △H=+77.0kJ?molˉ1(3分,焓变写错扣1分,用等号不扣分)
(2)0.003mol?Lˉ1?minˉ1(2分,单位写错0分) 6.75×10ˉ4(2分)
(3)C、D(共2分,只答对一个给1分,答错一个0分)
(4)O2+2H2O+4eˉ=4OHˉ或3O2+6H2O+12eˉ=12OHˉ(3分,电极反应式没配平0分) 负(2分) 6(2分)
解析试题分析:(1)根据盖斯定律可知,已知反应I+II可得:CH4(g)+ H2O(g)= CH3OH(g)+H2(g) △H=+77.0kJ?molˉ1;(2)CH4的起始浓度为1.0mol÷100L=0.01mol?Lˉ1,读图可知100℃时其平衡转化率为50%,则CH4的变化浓度为0.01mol?Lˉ1×50%=0.005mol?Lˉ1,则v(CH4)= 0.005mol?Lˉ1÷5min=0.001mol?Lˉ1?minˉ1,根据系数之比等于速率之比可知,v(H2)=3×v(CH4)= 0.003mol?Lˉ1?minˉ1;根据变化浓度之比等于系数之比,则反应I:
CH4(g) + H2O(g)  CO(g) + 3H2(g)
CO(g) + 3H2(g)
起始浓度/ mol?Lˉ1 0.01 0.01 0 0
变化浓度/ mol?Lˉ1 0.005 0.005 0.005 0.015
平衡浓度/ mol?Lˉ1 0.005 0.005 0.005 0.015
K=[c(CO)?c3(H2)]/[c(CH4)?c(H2O)]= [0.005×0.0153]/[ 0.005×0.005]=6.75×10ˉ4
(3)反应II是气态物质体积减小的反应,缩小容器体积,能增大各组分浓度,也能增大压强,平衡向正反应方向移动,但是平衡常数保持不变,因为温度不变平衡常数K不变,故A错误;同时增大反应物和生成物的浓度,正、逆反应速率均增大,但是v(正)>v(逆),所以平衡右移,故B错误;增大压强平衡右移,使生成物的量增加,故C正确;增大压强平衡向正反应方向移动,反应物浓度减小,生成物浓度增大,则重新平衡后反应物浓度/生成物浓度的值减小,故D正确;(4)甲醇完全燃烧生成CO2和H2O,CO2和过量KOH反应生成K2CO3和H2O,则该电池负极的主要反应物和产物分别是CH3OH、CO32ˉ,碳元素由-2价升为+4价,则CH3OH-6eˉ→CO32ˉ,由于KOH是强碱,应该用OHˉ使左右电荷守恒,则CH3OH-6eˉ+8OHˉ→CO32ˉ,根据氢、氧原子个数守恒可得,负极反应式为CH3OH-6eˉ+8OHˉ=CO32ˉ+6H2O或2CH3OH-12eˉ+16OHˉ=2CO32ˉ+12H2O;而正极的主要反应物是O2,同理可推断正极反应式为O2+2H2O+4eˉ=4OHˉ或3O2+6H2O+12eˉ=12OHˉ;放电时负极流出电子,正极流入电子,则阴离子移向负极,阳离子移向正极,则溶液中的OHˉ移向负极;根据系数之比等于物质的量之比,则1mol甲醇完全反应失去6mol电子,因此该燃料电池转移6mol电子。
考点:考查化学反应原理,涉及热化学方程式的书写、盖斯定律的应用、平均反应速率的计算、平衡转化率和化学平衡常数的计算、化学平衡、燃料电池的工作原理等知识。

 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案工业上可以利用废气中的CO2为原料制取甲醇,其反应方程式为:CO2+3H2 CH3OH+H2O。请回答下列问题:
CH3OH+H2O。请回答下列问题:
(1)已知常温常压下下列反应的能量变化如下图所示:
|
|
|
|

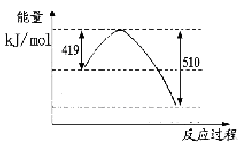 写出由二氧化碳和氢气制备甲醇的热化学方程式__ _。
写出由二氧化碳和氢气制备甲醇的热化学方程式__ _。该反应的△S____0(填“>”或“<”或“=”),在 ______情况下有利于该反应自发进行。
(2)如果上述反应方程式的平衡常数K值变大,则该反应__ (选填编号)。
A.一定向正反应方向移动 B.在平衡移动时正反应速率先增大后减小
C.一定向逆反应方向移动 D.在平衡移动时逆反应速率先减小后增大
(3)如果上述反应在体积不变的密闭容器中发生,能说明反应已达到平衡状态的是 __ (选填编号)。
A.3v正(H2)=v逆(CO2) B.C(H2) = C(CO2)
C.容器内气体的密度不变 D.容器内压强不变
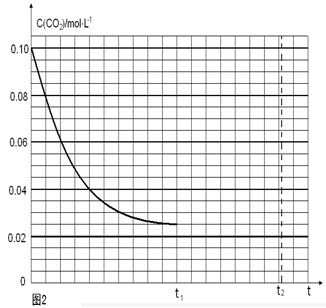
(4)若反应的容器容积为2.0L,反应时间4.0 min,容器内气体的密度增大了2.0g/L,在这段时间内CO2的平均反应速率为 。反应在t1时达到平衡,过程中c(CO2)随时间t变化趋势曲线右图所示。保持其他条件不变,t1时将容器体积压缩到1L,请画出t1后c(CO2)随时间t变化趋势曲线(t2达到新的平衡)。
工业制硫酸时,利用催化氧化反应将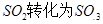 是一个关键的步骤。
是一个关键的步骤。
(1)某温度下,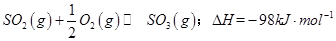 。开始时在100L的密闭容器中加入4.0molSO2(g)和10.0molO2,当反应达到平衡时共放出热量196kJ,该温度下平衡常数K=____________。
。开始时在100L的密闭容器中加入4.0molSO2(g)和10.0molO2,当反应达到平衡时共放出热量196kJ,该温度下平衡常数K=____________。
(2)一定条件下,向一带活塞的密闭容器中充入2mol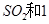 mol
mol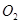 ,发生反应:
,发生反应: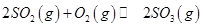 ,达平衡后改变下述条件,
,达平衡后改变下述条件, 气体平衡浓度都比原来增大的是____________(填字母)。
气体平衡浓度都比原来增大的是____________(填字母)。
A.保持温度和容器体积不变,充入2mol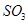 |
| B.保持温度和容器体积不变,充入2molN2 |
C.保持温度和容器内压强不变,充入1mol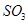 |
| D.移动活塞压缩气体 |
(3)下列关于
 反应的图像中,不正确的是_________。
反应的图像中,不正确的是_________。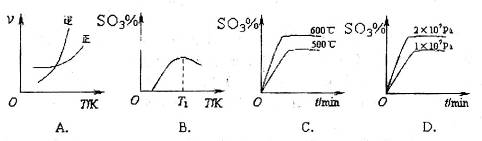
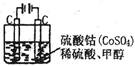
(4)同学们学习了电化学知识后大家提出,可以用电解的方法来生产硫酸,可避免产生酸雨,污染环境。于是大家设计了一个以铂为电极,两极分别通入SO2和空气,酸性电解液来实现电解生产硫酸。
①阳极的电极反应为______________________________。
②若电解液为2L0.025mol
 的硫酸溶液,当电解过程共转移了0.1mol电子时,理论上消耗SO2的体积为(标准状况)为_________,此溶液的pH="__________" (忽略溶液体积变化)。
的硫酸溶液,当电解过程共转移了0.1mol电子时,理论上消耗SO2的体积为(标准状况)为_________,此溶液的pH="__________" (忽略溶液体积变化)。 ③设计此实验的想法得到了老师的充分肯定,但与工业上生产硫酸相比还是有很多不足,请对此实验进行合理的评价____________________________(写出一点即可)。
(16分)某小组同学利用H2C2O4溶液和酸性KMnO4溶液反应来探究“条件对化学反应速率的影响”。实验时,先分别量取两种溶液,倒入大试管中迅速振荡混合均匀,再加入硫酸,开始计时,通过测定混合溶液褪色所需时间来判断反应的快慢(已知反应方程式为:5H2C2O4+2KMnO4+3H2SO4=2MnSO4+K2SO4+10CO2↑+8H2O)。该小组设计了如下方案。
| 编号 | H2C2O4溶液 | KMnO4溶液 | 硫酸溶液 | 温度/℃ | ||
| | 浓度 (mol/L) | 体积 (mL) | 浓度 (mol/L) | 体积 (mL) | | |
| ① | 0.10 | 2.0 | 0.010 | 4.0 | 4mL 4mol/L | 25 |
| ② | 0.20 | 2.0 | 0.010 | 4.0 | 4mL 4mol/L | 25 |
| ③ | 0.20 | 2.0 | 0.010 | 4.0 | 4mL 4mol/L | 50 |
(2)该小组同学由此实验发现反应进行一些时间后,有一时间段反应速率不断加快。同学们分析除了反应放热使体系温度升高外,可能还有其它原因,他们联想到教材上的科学探究实验,推断出反应混合溶液中的__________(填化学式)也加速了此反应的进行。
(3)上述实验①中充分反应后H2C2O4过量,假设理论上能通过用酸性KMnO4溶液滴定的方法来测定反应混合液中过量的H2C2O4,请回答下列问题:
①取用反应混合液的滴定管用__________滴定管(填“酸式”或“碱式”,下同),盛装KMnO4溶液的滴定管用__________滴定管。
②下列操作中可能使测出的H2C2O4剩余量比理论值偏低的是__________。
A.读取酸性KMnO4溶液体积时,开始仰视读数,滴定结束时俯视读数
B.滴定前盛放反应混合液的锥形瓶用蒸馏水洗净但没有干燥
C.盛装KMnO4溶液的滴定管滴定前有气泡,滴定后气泡消失
D.盛装KMnO4溶液的滴定管未润洗就直接注入酸性KMnO4溶液
③此滴定实验是否需要滴加指示剂________(填“是”或“否”);怎么确定此滴定的终点:_________。
 2C(g),达平衡后生成1.2mol C,平衡混合气体中C的体积分数为ω。
2C(g),达平衡后生成1.2mol C,平衡混合气体中C的体积分数为ω。 2Z(气),压强一定时,测得在平衡时Z的体积分数为0.4。
2Z(气),压强一定时,测得在平衡时Z的体积分数为0.4。
 CaO+2HBr ②2HBr+Hg
CaO+2HBr ②2HBr+Hg HgBr2+H2
HgBr2+H2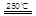 _____ + ④2HgO
_____ + ④2HgO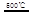 2Hg+O2↑
2Hg+O2↑ CO2(g)+H2(g) △H<0
CO2(g)+H2(g) △H<0