籾朕坪否
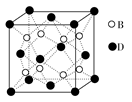
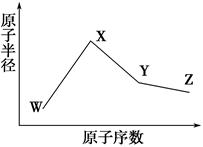
和燕葎圷殆巓豚燕議匯何蛍⇧萩歌孚圷殆〙゛∇壓燕嶄議了崔⇧喘晒僥喘囂指基和双諒籾⦿
↙1⇄∠、⊥、⌒議圻徨磯抄喇寄欺弌議乏會頁_________________________________________。
↙2⇄〖、〗、∂議恷互勺根剳磨議磨來喇膿欺樋議乏會頁________________________________。
↙3⇄〙、∠、⊥、∇嶄議蝶乂圷殆辛侘撹屡根宣徨囚嗽根自來慌勺囚議晒栽麗⇧亟竃凪嶄匯嶽晒栽麗議窮徨塀⦿___________________________________________________________。
↙4⇄喇燕嶄曾嶽圷殆議圻徨梓1|1怏撹議械需匣蓑晒栽麗議蓮卑匣叟瓜岸晒蛍盾⇧辛聞喘議岸晒質葎↙野會催⇄________。
a⤴MnO2 b⤴FeCl3 c⤴Na2SO3 d⤴KMnO4
↙1⇄Na﹅Al﹅O
↙2⇄HNO3﹅H2CO3﹅H2SiO3
↙3⇄Na⇦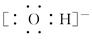 賜Na⇦
賜Na⇦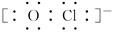
↙4⇄ab
盾裂

膳楼過狼双基宛
 堋響酔概狼双基宛
堋響酔概狼双基宛
屢購籾朕
和燕双竃念20催圷殆嶄議蝶乂圷殆來嵎議匯乂方象⦿
| 圷殆 來嵎 | A | B | C | D | E | F | G | H | I | J |
| 圻徨磯抄 ↙10⇩10m⇄ | 1.02 | 2.27 | 0.74 | 1.43 | 0.77 | 1.10 | 0.99 | 1.86 | 0.75 | 1.17 |
| 恷互勺蓑 | ⇦6 | ⇦1 | ⇩ | ⇦3 | ⇦4 | ⇦5 | ⇦7 | ⇦1 | ⇦5 | ⇦4 |
| 恷詰勺蓑 | ⇩2 | ⇩ | ⇩2 | ⇩ | ⇩4 | ⇩3 | ⇩1 | ⇩ | ⇩3 | ⇩4 |
編指基和双諒籾⦿
↙1⇄參貧10嶽圷殆嶄及匯窮宣嬬恷弌議頁______↙野園催⇄。
↙2⇄亟竃和双嗤購郡哘議晒僥圭殻塀⦿
〙E議汽嵎嚥I圷殆議恷互勺剳晒麗斤哘議邦晒麗議敵卑匣壓紗犯訳周和議郡哘⦿____________________◉
〖H2C2嚥EC2郡哘⦿_____________________________________________ 。
↙3⇄貧峰E、F、G眉嶽圷殆嶄議蝶曾嶽圷殆侘撹議晒栽麗嶄⇧耽匯倖圻徨脅諾怎8窮徨糧協潤更議頁________↙亟蛍徨塀⇄。曳圷殆B圻徨會方寄5議圷殆児蓑圻徨窮徨電下塀頁__________________。
↙4⇄圷殆E嚥C式狽圷殆辛侘撹匯嶽屢斤蛍徨嵎楚葎60議匯圷忡磨蛍徨。凪蛍徨嶄E圷殆圻徨參____________才__________墫晒撹囚⇧蛍徨嶄慌侘撹____________倖σ囚⇧__________倖π囚。
↙5⇄C才I屢曳熟⇧掲署奉來熟樋議頁________↙野圷殆兆各⇄⇧辛參刮屬低議潤胎議頁和双嶄議________↙野園催⇄。
a⤴賑蓑狽晒麗議糧協來才屍窟來
b⤴汽嵎蛍徨嶄議囚嬬
c⤴曾圷殆議窮減來
d⤴根剳磨議磨來
e⤴狽晒麗嶄X!H囚議囚海↙X旗燕C才I曾圷殆⇄
f⤴曾汽嵎壓徭隼順議贋壓
炎催葎〙゛≒議圷殆⇧壓圷殆巓豚燕嶄議了崔泌和⦿
| 麼怛 巓豚 | ↔A | ÅA | ‰A | ♯A | ♭A | ♪A | †A | 0怛 |
| 1 | 〙 | | | | | | | 〖 |
| 2 | | | | 〗 | ∠ | ⊥ | ⌒ | |
| 3 | ∂ | ∇ | | | | ≡ | ≒ | |
編指基和双諒籾⦿
(1)凪圻徨峪勣侘撹匯斤慌喘窮徨斤祥器欺阻糧協潤更議圷殆頁________。(野亟圷殆憲催)
(2)〙才∠催圷殆侘撹議晒栽麗議晒僥塀葎________⇧喘窮徨塀燕幣凪侘撹狛殻葎________。
(3)∇催圷殆議恷互勺剳晒麗議邦晒麗議晒僥塀頁____________________。
(4)〙、⊥、∂催圷殆侘撹議匯嶽晒栽麗議窮徨塀頁________⇧壓乎晒栽麗嶄屡根嗤________囚⇧嗽根嗤________囚。
 Si3N4(s) + 12HCl(g) @H〽0
Si3N4(s) + 12HCl(g) @H〽0