题目内容
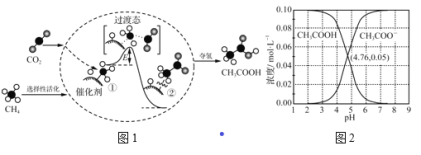
【题目】图1为CO2与CH4转化为CH3COOH的反应历程(中间体的能量关系如虚框中曲线所示),图2为室温下某溶液中CH3COOH和CH3COO-两种微粒浓度随pH变化的曲线。下列结论错误的是
A. CH4分子在催化剂表面会断开C—H键,断键会吸收能量
B. 中间体①的能量大于中间体②的能量
C. 室温下,CH3COOH的电离常数Ka=10-4.76
D. 升高温度,图2中两条曲线交点会向pH增大方向移动
【答案】D
【解析】
A.虚框内中间体的能量关系图可知,CH4分子在催化剂表面断开C-H键,断裂化学键需要吸收能量,A项正确;
B. 从虚框内中间体的能量关系图看,中间体①是断裂C—H键形成的,断裂化学键需要吸收能量,中间体②是形成C—C和O—H键形成的,形成化学键需要释放能量,所以中间体①的能量大于中间体②的能量,B项正确;
C.由图2可知,当溶液pH=4.76,c(CH3COOH)=c(CH3COO-)=0.05mol/L,CH3COOH![]() CH3COO-+H+的电离常数Ka=
CH3COO-+H+的电离常数Ka=![]() =c(H+)=10-4.76。C项正确;
=c(H+)=10-4.76。C项正确;
D.根据CH3COOH![]() CH3COO-+H+的电离常数Ka=
CH3COO-+H+的电离常数Ka=![]() 可知,图2两条曲线的交点的c(H+)值等于醋酸的电离常数Ka的值,而升高温度电离常数增大,即交点的c(H+)增大,pH将减小,所以交点会向pH减小的方向移动。D项错误;答案选D。
可知,图2两条曲线的交点的c(H+)值等于醋酸的电离常数Ka的值,而升高温度电离常数增大,即交点的c(H+)增大,pH将减小,所以交点会向pH减小的方向移动。D项错误;答案选D。

【题目】在100℃时,将0.2molN2O4(g)充入2L的恒容密闭容器中,间隔一定时间后对该容器内各物质的物质的量进行测定,得到如下数据:
时间/s | 0 | 20 | 40 | 60 | 80 |
N(N2O4)/mol | 0.20 | n1 | 0.10 | n3 | n4 |
N(NO2)/mol | 0.00 | 0.12 | n2 | 0.24 | 0.24 |
(1)该反应的平衡常数表达式为___________________________,由表中数据分析可得,n1=____mol,n3=________________mol;
(2)在上述条件下,从0到40s内NO2的平均反应速率为___________________;
(3)该反应达到化学平衡后,下列改变可使N2O4浓度增大的是_____(填序号);
A.增大容器的容积 B.向容器中充入一定量的NO2
C.向容器中再充入一定量的N2O4 D.向容器中充入一定量的He(g)
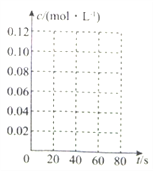
(4)在下图中画出此反应中N2O4的浓度随时间变化的曲线_________。